
Wetenschap
Het oplossende vermogen van water:polaire moleculen begrijpen
Polaire moleculen:
* Ionische verbindingen: Deze worden bij elkaar gehouden door elektrostatische krachten tussen positief en negatief geladen ionen. Door de polariteit van water kan het deze ionen omringen en scheiden, waardoor ze uiteenvallen. Voorbeelden hiervan zijn tafelzout (NaCl), suiker (sucrose) en veel zouten.
* Polaire covalente verbindingen: Deze delen de elektronen ongelijk, waardoor een gedeeltelijk positieve en gedeeltelijk negatieve lading binnen het molecuul ontstaat. De polariteit van water heeft een wisselwerking met deze ladingen, waardoor waterstofbruggen worden gevormd en deze kunnen oplossen. Voorbeelden zijn onder meer ethanol, glucose en veel organische zuren.
Niet-polaire moleculen:
* Hoewel water vooral goed is in het oplossen van polaire moleculen, kan het sommige niet-polaire moleculen in beperkte mate oplossen. Dit komt door de zwakke interacties die Londense dispersiekrachten worden genoemd. Dit zijn tijdelijke fluctuaties in de elektronenverdeling die tot zwakke aantrekkingen kunnen leiden. Voorbeelden zijn onder meer zuurstofgas (O2), stikstofgas (N2) en enkele kleine koolwaterstoffen.
Factoren die de oplosbaarheid beïnvloeden:
* Polariteit: Zoals hierboven vermeld:hoe polairder een molecuul is, des te beter oplosbaar het zal zijn in water.
* Temperatuur: Het verhogen van de temperatuur verhoogt over het algemeen de oplosbaarheid, omdat moleculen meer energie hebben om aantrekkingskrachten te overwinnen en op te lossen.
* Druk: Druk heeft een groter effect op de oplosbaarheid van gassen in vloeistoffen dan op de oplosbaarheid van vaste stoffen.
* Intermoleculaire krachten: De sterkte van de krachten tussen watermoleculen en de opgeloste moleculen beïnvloedt de oplosbaarheid.
Voorbeelden van moleculen die in water oplossen:
* Suikers: Net als sucrose zijn glucose en fructose polaire moleculen en lossen ze gemakkelijk op in water.
* Zouten: Veel zouten, zoals natriumchloride, lossen op in water en vormen ionen.
* Zuren en basen: Veel zuren en basen zijn polaire moleculen en lossen gemakkelijk op in water.
* Alcoholen: Ethanol en andere alcoholen zijn polaire moleculen die goed in water oplossen.
Het is belangrijk om te onthouden dat sommige moleculen niet oplosbaar zijn in water, ook al zijn ze polair. Olie en water mengen bijvoorbeeld niet omdat de niet-polaire oliemoleculen niet worden aangetrokken door de polaire watermoleculen.
 Als ademhaling koolstofdioxide en water produceert, wat gebeurt er dan met deze producten voor dat ze in het lichaam worden opgebouwd?
Als ademhaling koolstofdioxide en water produceert, wat gebeurt er dan met deze producten voor dat ze in het lichaam worden opgebouwd?  Hoe noem je die gasstreamer tussen zonnevlekken?
Hoe noem je die gasstreamer tussen zonnevlekken?  Wat is de theorie van redoxtitratie?
Wat is de theorie van redoxtitratie?  Is ammoniumnitriet zuur of basisch?
Is ammoniumnitriet zuur of basisch?  Vergelijking voor loodnitraat en calciumjodide worden gecombineerd?
Vergelijking voor loodnitraat en calciumjodide worden gecombineerd?
 Het ozongat in Antarctica is een van de grootste en diepste van de afgelopen jaren
Het ozongat in Antarctica is een van de grootste en diepste van de afgelopen jaren Plasticvervuiling:kunnen we de oceaan opruimen met technologie?
Plasticvervuiling:kunnen we de oceaan opruimen met technologie? Nieuw boek laat zien hoe het oude Griekse schrift ons helpt de huidige milieucrises te begrijpen
Nieuw boek laat zien hoe het oude Griekse schrift ons helpt de huidige milieucrises te begrijpen  Dronetechnologie biedt nieuwe manieren om klimaatverandering te beheersen
Dronetechnologie biedt nieuwe manieren om klimaatverandering te beheersen Hoe bittere koude winteruitbarstingen en een opwarmende planeet de kustlijn van Lake Michigan zullen opvreten?
Hoe bittere koude winteruitbarstingen en een opwarmende planeet de kustlijn van Lake Michigan zullen opvreten?
Hoofdlijnen
- Waarom evolutie sommige cellen tot altruïsme drijft
- Welk land kloneert het meest?
- Wat is de wetenschappelijke naam voor rot weg?
- Is dermatameculitis een deel van de wetenschap?
- Welke organel heeft membraangebonden structuren in een cel die gespecialiseerde functies uitvoeren?
- Wat betekenen gegevens in het wetenschapsproject?
- Effecten van de toevoer van organisch materiaal en temperatuurverandering op de met bodemaggregaten geassocieerde ademhaling en microbieel koolstofgebruik
- Alleen structuren betrokken bij mitose van dierlijke cellen?
- Wat is Biogeocycle?
- Bepalen of een oplossing neutraal, basisch of zuur is (pH-identificatietechnieken)

- Zwitsers zakmeskatalysator kan aardgas schoner maken
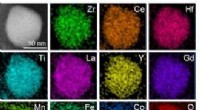
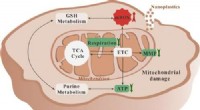
- Nanoplastics kunnen menselijke lever- en longcelprocessen verstoren in laboratoriumexperimenten
- Onderzoekers ontwikkelen een manier om corrosie door ruwe olie beter te voorspellen

- Video:Hoeveel weegt een wolk?

 Hoe ondersteunt de ouderdom van gesteenten op de zeebodem de verspreiding van de theorie?
Hoe ondersteunt de ouderdom van gesteenten op de zeebodem de verspreiding van de theorie?  Welk element heeft de elektronische structuur 2.7?
Welk element heeft de elektronische structuur 2.7?  Er zijn gegevens gevonden over de overlevenden van Pompeii; archeologen beginnen te begrijpen hoe zij hun leven opnieuw hebben opgebouwd
Er zijn gegevens gevonden over de overlevenden van Pompeii; archeologen beginnen te begrijpen hoe zij hun leven opnieuw hebben opgebouwd  Is een stok van dynamiet een voorbeeld van kinetische energie?
Is een stok van dynamiet een voorbeeld van kinetische energie?  Hoe is de zomer op Uranus?
Hoe is de zomer op Uranus?  Wat gebeurt er als snelheid negatief is en versnellingspositief is?
Wat gebeurt er als snelheid negatief is en versnellingspositief is?  Noem het extra product gevormd wanneer een zuur wordt geneutraliseerd door antacida dat een carbonaat of bicarbonaat bevat?
Noem het extra product gevormd wanneer een zuur wordt geneutraliseerd door antacida dat een carbonaat of bicarbonaat bevat?  Welk celorganel regelt de synthese van enzymen?
Welk celorganel regelt de synthese van enzymen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

