
Wetenschap
Berekening van de pH van een KOH-oplossing:een stapsgewijze handleiding
1. Bereken het aantal mol KOH:
* Molar massa van KOH: 39,10 g/mol (K) + 16,00 g/mol (O) + 1,01 g/mol (H) =56,11 g/mol
* Mollen KOH: (0,140 g KOH) / (56,11 g/mol) =0,00250 mol KOH
2. Bereken de concentratie van KOH:
* Concentratie (Molariteit): (0,00250 mol KOH) / (0,250 L oplossing) =0,0100 M KOH
3. Begrijp de dissociatie van KOH:
* KOH is een sterke base, wat betekent dat het volledig dissocieert in water:
KOH(aq) → K+(aq) + OH-(aq)
* Dit betekent dat de concentratie OH-ionen gelijk is aan de concentratie KOH.
4. Bereken de pOH:
* pOH: -log[OH-] =-log(0,0100) =2,00
5. Bereken de pH:
* pH + pOH =14
* pH =14 - pOH =14 - 2,00 =12,00
Daarom is de pH van de oplossing 12,00.
 Satellieten laten zien dat orkaan Gert wordt getroffen door windschering
Satellieten laten zien dat orkaan Gert wordt getroffen door windschering Griekenland verhoogt het waarschuwingsniveau voor natuurbranden na een golf van branden
Griekenland verhoogt het waarschuwingsniveau voor natuurbranden na een golf van branden  Kokende hitte en geen water:kranen lopen droog in Zuid-Irak
Kokende hitte en geen water:kranen lopen droog in Zuid-Irak De toxiciteit van banden wordt opnieuw onder de loep genomen na het afsterven van zalm
De toxiciteit van banden wordt opnieuw onder de loep genomen na het afsterven van zalm  Sleepbare sensor vrije val om verticale delen van oceaanomstandigheden te meten
Sleepbare sensor vrije val om verticale delen van oceaanomstandigheden te meten
Hoofdlijnen
- Methionine:de sleutel tot eiwitsynthese - hoe het werkt
- De cel is afhankelijk van externe bronnen van organische moleculen die kunnen worden gebruikt om energie te produceren omdat?
- Welke organismen ondergaan zowel fotosynthese als cellulaire ademhaling?
- Wat is anatomie?
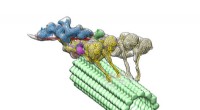
- Onderzoekers verkrijgen een momentopname die verduidelijkt hoe materialen cellen binnendringen
- Hoe groeit en ontwikkelt het menselijk embryo?
- Wat betekent Piggy met zijn bewering dat het leven wetenschappelijk is?
- Hoe noteer ik een Karyotype
- Wisseling van de wacht - onderzoek werpt licht op hoe planten ademen
- Een methode om onbekende moleculen van koraalriffen te screenen op hun therapeutisch potentieel

- Microscopische strijdwagens leveren moleculen in onze cellen
- Begrijpen wat zwart pigment zwart maakt

- Het gebruik van materiaal met een hoge energiedichtheid in het ontwerp van de elektrode verbetert lithiumzwavelbatterijen

- Vogelveren inspireren onderzoekers om levendige nieuwe kleuren te produceren

 Mengsels die niet gelijkmatig worden gemengd maar niet gemakkelijk kunnen worden gescheiden door te filteren -a -Alys-B-Suspensions-Colloids-D-Solutions?
Mengsels die niet gelijkmatig worden gemengd maar niet gemakkelijk kunnen worden gescheiden door te filteren -a -Alys-B-Suspensions-Colloids-D-Solutions?  Wat is de juiste chemische naam voor CAI2?
Wat is de juiste chemische naam voor CAI2?  Watts gebruikt door industriële machines
Watts gebruikt door industriële machines De levende wereld boven ons hoofd:hoe stadsbomen de biodiversiteit helpen vormgeven
De levende wereld boven ons hoofd:hoe stadsbomen de biodiversiteit helpen vormgeven  lanceerden de eerste zelfgebouwde satelliet van Australië, en het is een gigantische sprong naar de maan
lanceerden de eerste zelfgebouwde satelliet van Australië, en het is een gigantische sprong naar de maan Beheers geheugen- en weergavefuncties op uw wetenschappelijke rekenmachine
Beheers geheugen- en weergavefuncties op uw wetenschappelijke rekenmachine  Hoe komt silicium voor?
Hoe komt silicium voor?  Voors en tegens van synthetische polymeren
Voors en tegens van synthetische polymeren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

