
Wetenschap
Hydrobroomzuur (HBr) dissociatie in water:chemische vergelijking en uitleg
Broomwaterstofzuur (HBr) is een sterk zuur, wat betekent dat het volledig ioniseert in water. De vergelijking voor de reactie met water is:
HBr (aq) + H₂O (l) → H₃O⁺ (aq) + Br⁻ (aq)
Dit is wat de vergelijking vertegenwoordigt:
* HBr (aq): Waterstofbromide in waterige oplossing.
* H₂O (l): Vloeibaar water.
* H₃O⁺ (aq): Hydroniumion, de vorm waarin waterstofionen (H⁺) in water voorkomen.
* Br⁻ (aq): Bromide-ion, het anion dat wordt gevormd wanneer HBr ioniseert.
Uitleg:
Wanneer broomwaterstofzuur in water wordt opgelost, doneert het een proton (H⁺) aan een watermolecuul, waardoor een hydroniumion (H₃O⁺) en een bromide-ion (Br⁻) wordt gevormd. Dit proces wordt ionisatie genoemd en resulteert in een zure oplossing.
 Wat betekent fysisch en chemisch in de wetenschap?
Wat betekent fysisch en chemisch in de wetenschap?  Patterning-methode kan de weg vrijmaken voor nieuwe op glasvezel gebaseerde apparaten, slim textiel
Patterning-methode kan de weg vrijmaken voor nieuwe op glasvezel gebaseerde apparaten, slim textiel Wat is het oplosmiddel en de opgeloste stof voor het ontsmetten van alcohol?
Wat is het oplosmiddel en de opgeloste stof voor het ontsmetten van alcohol?  Waarom zout dodelijk is voor bloedzuigers
Waarom zout dodelijk is voor bloedzuigers Wat zijn twee eigenschappen van covalente verbindingen?
Wat zijn twee eigenschappen van covalente verbindingen?
Hoofdlijnen
- Hoeveel soorten planten zijn vleesetend?
- Is een huidmondcel een dierencel?
- Vogelgriep bij rundvee:wat zijn de zorgen rond het nieuw opkomende rundergriepvirus H5N1?
- Hoe belangrijk is een wetenschapper zijn?
- Zijn aminozuren een nucleïnezuur?
- In de biologie die hun eigen eten maakt?
- Welke organel is de elektriciteitscentrale van cel?
- Berekening van de tijd voor celverdubbeling
- Is Cynobacteria het eerste levende organisme op aarde?
- Russische wetenschappers ontwikkelen een slim sorptiemiddel voor waterzuivering

- Chili-vormig apparaat zou kunnen onthullen hoe heet die peper is
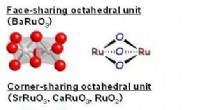
- Bariumruthenaat:een hoog rendement, gemakkelijk te hanteren perovskietkatalysator voor de oxidatie van sulfiden
- Nauwkeurig gedefinieerde polymeerketens nu een realiteit

- Nieuwe behandelingstechnologie kan de belasting van nucleair afval in het VK verminderen
 Wanneer twee aminozuren combineren, doet de groep van één molecuul met zuur tweede molecuul?
Wanneer twee aminozuren combineren, doet de groep van één molecuul met zuur tweede molecuul?  Hoe lang stroomt de warmte -energie?
Hoe lang stroomt de warmte -energie?  Het is maïs! Hoe de online virale 'Corn Kid' op weg is naar roem in de kinderinfluencer-industrie
Het is maïs! Hoe de online virale 'Corn Kid' op weg is naar roem in de kinderinfluencer-industrie  Welke oorzaken metamorf gesteente vormen
Welke oorzaken metamorf gesteente vormen  De structuur van RNA ontdekken
De structuur van RNA ontdekken Spelt of zachte tarwe? Hun diversiteit aan voedingscomponenten verhindert de identificatie welke soort gezonder is
Spelt of zachte tarwe? Hun diversiteit aan voedingscomponenten verhindert de identificatie welke soort gezonder is  Hoe sterk is de zwaartekracht op elke planeet?
Hoe sterk is de zwaartekracht op elke planeet?  Nieuw flexibel, transparante geleider gemaakt:opvouwbare flatscreen-tv's dichter bij de realiteit
Nieuw flexibel, transparante geleider gemaakt:opvouwbare flatscreen-tv's dichter bij de realiteit
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

