
Wetenschap
Oxaalzuur in conductometrische titraties:eigenschappen en toepassingen
1. Goed gedefinieerde dissociatie: Oxaalzuur heeft twee verschillende dissociatiestappen met bekende evenwichtsconstanten. Dit maakt de identificatie mogelijk van twee duidelijke equivalentiepunten in de conductometrische titratie, waardoor deze geschikt is voor de bepaling van zowel de eerste als de tweede dissociatieconstante.
2. Hoge zuiverheid en stabiliteit: Oxaalzuur is gemakkelijk verkrijgbaar in hoge zuiverheid en is stabiel in oplossing, waardoor nauwkeurige en betrouwbare titratieresultaten worden gegarandeerd.
3. Bekende molaire massa: De molaire massa van oxaalzuur is goed gedefinieerd, waardoor nauwkeurige berekeningen mogelijk zijn van de concentratie van de onbekende oplossing die wordt getitreerd.
4. Gemakkelijk oplosbaar: Oxaalzuur lost gemakkelijk op in water, waardoor de bereiding van standaardoplossingen voor titratie wordt vergemakkelijkt.
5. Geschikt voor verschillende titranten: Oxaalzuur kan worden gebruikt voor titraties met een verscheidenheid aan basen, waaronder sterke basen zoals natriumhydroxide (NaOH) en zwakkere basen zoals ammoniak (NH₃).
Hoe het werkt bij conductometrische titratie:
Conductometrische titratie is gebaseerd op het meten van veranderingen in de geleidbaarheid van de oplossing tijdens de titratie. Terwijl de titrant wordt toegevoegd, interageren de in de oplossing aanwezige ionen, wat leidt tot veranderingen in de geleidbaarheid.
* Eerste oplossing: De initiële oplossing die oxaalzuur bevat, heeft een lage geleidbaarheid vanwege de lage concentratie ionen (H⁺ en oxalaationen).
* Titratie met basis: Als er een base wordt toegevoegd, reageert deze met het oxaalzuur, neutraliseert het en genereert meer ionen (bijvoorbeeld Na⁺ en OH⁻). Dit leidt tot een toename van de geleidbaarheid.
* Equivalentiepunt: Op het equivalentiepunt is al het oxaalzuur geneutraliseerd, waardoor een maximale geleidbaarheid ontstaat.
* Voorbij het gelijkwaardigheidspunt: Verdere toevoeging van base verhoogt alleen de concentratie van OH⁻-ionen, wat leidt tot een geleidelijke toename van de geleidbaarheid.
Over het geheel genomen biedt het gebruik van oxaalzuur bij conductometrische titraties een betrouwbare en gemakkelijke methode voor het bepalen van de concentratie van onbekende oplossingen, vooral die met zwakke zuren of basen.
 Waarom zijn verbindingen goede isolatoren?
Waarom zijn verbindingen goede isolatoren?  Hoeveel neutronen en elektronen zijn aanwezig in 19 fluor 16 zuurstof?
Hoeveel neutronen en elektronen zijn aanwezig in 19 fluor 16 zuurstof?  Wat is de grootte van natriumatoom?
Wat is de grootte van natriumatoom?  Koffiedik kan een sleutelrol spelen bij het voorkomen van neurodegeneratieve ziekten
Koffiedik kan een sleutelrol spelen bij het voorkomen van neurodegeneratieve ziekten  Aluminosilicaatglazen kunnen dienen als zichtbare luminescentiematerialen
Aluminosilicaatglazen kunnen dienen als zichtbare luminescentiematerialen
 Ondiepe sodameren zijn veelbelovend als bakermat van het leven op aarde
Ondiepe sodameren zijn veelbelovend als bakermat van het leven op aarde  De cryosfeer van de aarde is van vitaal belang voor iedereen
De cryosfeer van de aarde is van vitaal belang voor iedereen Terwijl we ons fixeren op het coronavirus, De aarde raast op een catastrofe af die erger is dan het uitsterven van de dinosauriërs
Terwijl we ons fixeren op het coronavirus, De aarde raast op een catastrofe af die erger is dan het uitsterven van de dinosauriërs Microplastics uit de wasmachine
Microplastics uit de wasmachine Door de mens veroorzaakt geluid kan van invloed zijn op de manier waarop dieren informatie uit geuren gebruiken
Door de mens veroorzaakt geluid kan van invloed zijn op de manier waarop dieren informatie uit geuren gebruiken
Hoofdlijnen
- Wat is de conclusie van onderlinge afhankelijkheid tussen levende organismen en milieu?
- Microbieel ecosysteem bij Laguna La Brava kan nieuwe micro-organismen bevatten
- CRISPR helpt onderzoekers ontdekken hoe koralen zich aanpassen aan de opwarming van de oceanen
- Wat zijn cellen die vreemde cellen opeten?
- Wat is de naam van de interne secretoire klieren van de wetenschap?
- Welk type cel wordt geproduceerd door de lange botten?
- Moet ik pompoentaart in de koelkast bewaren? Voedselveiligheidsinformatie voor het pompoenseizoen
- Wat is een afgesloten container voor het kweken en weergeven van levende dieren of planten?
- Planten kunnen zichzelf verdedigen door rupsen kannibaal te maken
- Wetenschappers suggereren een milieuvriendelijke manier om zeer actieve katalysatoren te verkrijgen

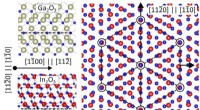
- Nieuw katalytisch effect ontdekt voor de productie van galliumoxide
- Chemici helpen kans een handje

- Cheminformatics-benaderingen voor het maken van nieuwe haarkleurmiddelen

- Big data-techniek onthult voorheen onbekende mogelijkheden van veelgebruikte materialen

 Vinders ontdekken Dark Mode in Android Q-lek
Vinders ontdekken Dark Mode in Android Q-lek China verbiedt nepnieuws gemaakt met AI, bots
China verbiedt nepnieuws gemaakt met AI, bots Akoestiek gebruiken om objecten te verbergen en te simuleren
Akoestiek gebruiken om objecten te verbergen en te simuleren De minst bruikbare vorm van energie is?
De minst bruikbare vorm van energie is?  Hoe nieuw bewijs van geslachtsomkeringen laat zien hoe chromosomen in de loop van de evolutionaire tijd in stand worden gehouden
Hoe nieuw bewijs van geslachtsomkeringen laat zien hoe chromosomen in de loop van de evolutionaire tijd in stand worden gehouden  Biodiversiteit:kunnen we waarde hechten aan de natuur?
Biodiversiteit:kunnen we waarde hechten aan de natuur? Hacker gebruikte Raspberry Pi-computer om beperkte NASA-gegevens te stelen
Hacker gebruikte Raspberry Pi-computer om beperkte NASA-gegevens te stelen Berkeley-onderzoekers verlichten witte OLED's
Berkeley-onderzoekers verlichten witte OLED's
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

