
Wetenschap
Atoomgrootte en lading:de atomaire structuur begrijpen
Hier is een overzicht:
* Neutraal atoom: In een neutraal atoom is het aantal protonen (positieve lading) gelijk aan het aantal elektronen (negatieve lading). De elektronen zijn verdeeld in energieniveaus (schillen) rond de kern. De buitenste schil bepaalt de grootte van het atoom.
* Kationen (positief geladen): Wanneer een atoom een elektron verliest, wordt het een kation. Dit verlies van een elektron vermindert de elektron-elektron-afstoting, wat leidt tot een kleinere atomaire straal. De buitenste schil bevindt zich nu dichter bij de kern, omdat deze door minder elektronen wordt beschermd.
* Anionen (negatief geladen): Wanneer een atoom een elektron krijgt, wordt het een anion. Het toegevoegde elektron verhoogt de elektron-elektronafstoting, wat leidt tot een grotere atomaire straal. De buitenste schil bevindt zich nu verder van de kern vanwege de toegenomen elektron-elektronenafstoting.
Daarom wordt de grootte van een atoom voornamelijk beïnvloed door het aantal elektronenschillen en de effectieve nucleaire lading die de buitenste elektronen ervaren.
Belangrijkste punten:
* Kationen zijn over het algemeen kleiner dan hun neutrale atomen.
* Anionen zijn over het algemeen groter dan hun neutrale atomen.
* De grootte van een atoom wordt niet alleen bepaald door zijn lading.
Voorbeeld:
* Natriumatoom (Na) heeft een grotere straal dan natriumion (Na+).
* Chlooratoom (Cl) heeft een kleinere straal dan chloride-ion (Cl-).
Samenvattend:hoewel het waar is dat kationen over het algemeen kleiner zijn dan hun neutrale atomen, en anionen groter, is de grootte van een atoom een complex samenspel van factoren.
Hoofdlijnen
- Welk lichaamssysteem is verantwoordelijk voor de reproductie?
- Wat is een voorbeeld van evolutie vandaag?
- Wat is de rol van DNA -moleculen in synthese -eiwitten?
- Waar in het lichaam wordt lipase geproduceerd?
- Klimaatverandering kan het mariene milieu meer dan wat dan ook beïnvloeden
- Is biotechnologie een deel van de chemie?
- Wat is het doel van het kleuren van een onbekend organisme?
- Wat is een Candium?
- Plaats van secretoire en membraaneiwitsynthese?
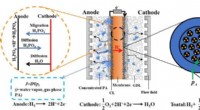
- Het voorspellen van de distributie van fosforzuur en water in een hoge-temperatuur polymeer elektrolytmembraan brandstofcel
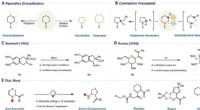
- Een reactie die zwavel verwijdert, stikstof- of zuurstofatomen uit zesledige ringen die alleen blauw licht gebruiken
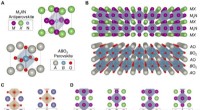
- Epitaxiale antiperovskiet/perovskiet heterostructuren voor materiaalontwerp
- Een betere manier om acryl te maken

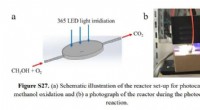
- Efficiëntie in fotokatalyse bleek plaatsgevoelig te zijn
 Welk type energie zet een windturbine om in elektrische energie?
Welk type energie zet een windturbine om in elektrische energie?  Audio-overkill? Sommigen twijfelen aan de voordelen van muziek in hoge resolutie
Audio-overkill? Sommigen twijfelen aan de voordelen van muziek in hoge resolutie  Hoe sociale media de consumentenbestedingen beïnvloeden
Hoe sociale media de consumentenbestedingen beïnvloeden  Wat is een systeem in wetenschappelijke termen?
Wat is een systeem in wetenschappelijke termen?  Kan een evenwichtige kracht de ruststatus of beweging een object veranderen?
Kan een evenwichtige kracht de ruststatus of beweging een object veranderen?  Hoe wordt onzuiver koper gezuiverd?
Hoe wordt onzuiver koper gezuiverd?  Wat zijn de niet -hernieuwbare brandstoffen beginnen met de zon als primaire energiebron?
Wat zijn de niet -hernieuwbare brandstoffen beginnen met de zon als primaire energiebron?  Welke planeet is dichter bij de zon en heeft kraters?
Welke planeet is dichter bij de zon en heeft kraters?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


