
Wetenschap
Ionische obligaties:de elektrostatische aantrekkingskracht tussen atomen begrijpen
Hier is een overzicht:
* Elektrostatische aantrekkingskracht: Dit verwijst naar de aantrekkingskracht tussen tegengesteld geladen objecten.
* Atomen met tegengestelde ladingen: In een ionische binding verliest één atoom (het metaal) elektronen en wordt het positief geladen (kation), terwijl het andere atoom (het niet-metaal) elektronen krijgt en negatief geladen wordt (anion).
Belangrijkste kenmerken van ionische bindingen:
* Sterke banden: Ionische bindingen zijn over het algemeen sterk vanwege de sterke elektrostatische aantrekkingskracht tussen de ionen.
* Hoge smelt- en kookpunten: De sterkte van de bindingen betekent dat ionische verbindingen doorgaans hoge smelt- en kookpunten hebben.
* Vast bij kamertemperatuur: De meeste ionische verbindingen zijn vast bij kamertemperatuur.
* Elektriciteit geleiden in vloeibare of waterige oplossingen: Wanneer ze worden opgelost of gesmolten, kunnen de ionen vrij bewegen, waardoor ze elektriciteit kunnen geleiden.
Voorbeeld:
Natriumchloride (NaCl) is een klassiek voorbeeld van een ionische verbinding. Natrium (Na) verliest een elektron om een positief geladen natriumion (Na+) te worden, en chloor (Cl) krijgt een elektron om een negatief geladen chloride-ion (Cl-) te worden. De elektrostatische aantrekkingskracht tussen deze tegengesteld geladen ionen vormt de ionische binding die de verbinding bij elkaar houdt.
 Oplossen van spanning op het oppervlak van polymeermengsels
Oplossen van spanning op het oppervlak van polymeermengsels Wetenschappers onderzoeken de chemie van een enkel batterij-elektrodedeeltje, zowel van binnen als van buiten
Wetenschappers onderzoeken de chemie van een enkel batterij-elektrodedeeltje, zowel van binnen als van buiten Hoeveel kernelektronen zijn er in broom?
Hoeveel kernelektronen zijn er in broom?  Hoe goed elektronentransport werkt in furfuralbiogas
Hoe goed elektronentransport werkt in furfuralbiogas  Kan zilver zink uit zijn zoutoplossing verdringen?
Kan zilver zink uit zijn zoutoplossing verdringen?
 Welke rol speelt de mens in een ecosysteem?
Welke rol speelt de mens in een ecosysteem?  Is de afname van de oppervlaktewindsnelheid in China geëindigd?
Is de afname van de oppervlaktewindsnelheid in China geëindigd? Moderne rekenkracht kan toekomstige overstromingsrampen helpen verminderen
Moderne rekenkracht kan toekomstige overstromingsrampen helpen verminderen De onderwateroerwouden van de zee geven helderder water
De onderwateroerwouden van de zee geven helderder water Biochar kan de anaërobe vergisting van dierlijke mest ten goede komen
Biochar kan de anaërobe vergisting van dierlijke mest ten goede komen
Hoofdlijnen
- Wat zijn drie belangrijke verschillen tussen de structuren van DNA en RNA?
- Waarom is het belangrijk dat organismen van dezelfde soort diversiteitsgenen hebben?
- Wat zijn de drie delen van fotosynthese?
- De celtheorie was het gevolg van het werk van wie?
- In welk proces gebruikt de cel blaasjes om het molecuul naar buiten te verplaatsen?
- Wat zijn de drie basisdelen van een dier en een plantencel?
- Welk lichaamssysteem produceert hormonen om orgelactiviteit te reguleren?
- Het ontdekken van één reden waarom zwermen evolueerden, biedt verleidelijke aanwijzingen over hoe intelligentie zich ontwikkelde
- Waarom maakt mijn kat me zo vroeg wakker en wat kan ik eraan doen?
- Door nieuwe technologie kunnen belangrijke metalen efficiënter worden gemaakt

- Een schijnwerper schijnen op de machinerie van het leven
- N-C-bindingen rechtstreeks vanuit distikstof maken:samenvatting en perspectief

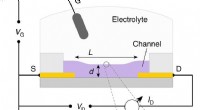
- Nieuwe methode benchmarkt organische gemengde geleiders
- Het maken van nepvlees roept vragen op over de gezondheid, ethiek en duurzaamheid voor een voormalige slager

 Geluid en licht gevangen door wanorde
Geluid en licht gevangen door wanorde Wat is een meteorietriem?
Wat is een meteorietriem?  Wat is de term voor rots die is verweerd om grond te worden?
Wat is de term voor rots die is verweerd om grond te worden?  Is metaaldraad een ohm -geleider?
Is metaaldraad een ohm -geleider?  Hubble detecteert exokometen die een duik nemen in een jonge ster
Hubble detecteert exokometen die een duik nemen in een jonge ster Wat is de tijdsverschillen van Kansas naar Georiga?
Wat is de tijdsverschillen van Kansas naar Georiga?  Archeoloog zet tanden in het begrijpen van culturele identiteit, interacties in de oude Nijlvallei
Archeoloog zet tanden in het begrijpen van culturele identiteit, interacties in de oude Nijlvallei Hoe leren geologen hoe een rots vormde?
Hoe leren geologen hoe een rots vormde?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

