
Wetenschap
Lewis-structuur van P₄O₁₀:een stapsgewijze handleiding
1. Valentie-elektronen tellen:
* Fosfor (P) heeft 5 valentie-elektronen en er zijn 4 fosforatomen, dus 5 * 4 =20 elektronen.
* Zuurstof (O) heeft 6 valentie-elektronen en er zijn 10 zuurstofatomen, dus 6 * 10 =60 elektronen.
* Totaal valentie-elektronen:20 + 60 =80 elektronen
2. Bepaal de centrale atoom(en):
* Fosfor is minder elektronegatief dan zuurstof en zal dus het centrale atoom zijn.
3. Verbind de atomen met enkele obligaties:
* Verbind de vier fosforatomen in een tetraëdrische vorm.
* Verbind elk fosforatoom met drie zuurstofatomen.
4. Verdeel de resterende elektronen:
* Je hebt 12 enkele bindingen gebruikt (12 * 2 =24 elektronen), waardoor er 56 elektronen overblijven.
* Plaats alleenstaande paren op elk zuurstofatoom om hun octetten te voltooien (8 elektronen rond elke zuurstof). Je gebruikt hiervoor 48 elektronen.
* Plaats de overige 8 elektronen als alleenstaande paren op de fosforatomen.
5. Controleer formele kosten:
* De formele lading op elk atoom moet tot een minimum worden beperkt. De fosforatomen hebben een formele lading +1 en de zuurstofatomen met enkele bindingen hebben een formele lading -1. De zuurstofatomen met dubbele bindingen hebben een formele lading van 0.
Eindstructuur:
De Lewis-structuur van P4O10 zal hebben:
* Vier centrale fosforatomen gerangschikt in een tetraëdrische vorm.
* Elk fosforatoom verbonden met drie zuurstofatomen.
* Twee van de zuurstofatomen die met elk fosforatoom verbonden zijn, zijn verbonden met dubbele bindingen, en één is verbonden met een enkele binding.
* Elk zuurstofatoom heeft twee vrije elektronenparen.
* Elk fosforatoom heeft één vrij elektronenpaar.
Belangrijke opmerking: Terwijl de Lewis-structuur de binding helpt visualiseren, heeft P4O10 een complexere 3D-structuur, waarbij de fosforatomen een tetraëder vormen en de zuurstofatomen daartussen een brug vormen.
 Waar zijn de boomhorizons van de boom uit?
Waar zijn de boomhorizons van de boom uit?  Modellering leidt tot een beter begrip van de rol die El Niño speelt bij toenemende regenval langs de kust van de Rode Zee
Modellering leidt tot een beter begrip van de rol die El Niño speelt bij toenemende regenval langs de kust van de Rode Zee Groeit schimmel sneller in het licht of donker?
Groeit schimmel sneller in het licht of donker?  Zelfgemaakt Bobcat-aas
Zelfgemaakt Bobcat-aas  Wat voor soort planten groeien op plaatsen met veel regen en water?
Wat voor soort planten groeien op plaatsen met veel regen en water?
Hoofdlijnen
- Wat is de taak van klieren in het mannelijke reproductieve systeem?
- Hoe overleven soorten evolueren en creëren ze speciatie?
- Hoe Gamete Fusion een diploïde zygote creëert
- Hoe ziet en dierencel eruit?
- Hoe wordt de suiker in RNA genoemd?
- Hoe beïnvloedt een gen de eigenschappen van Himan?
- Welk gebied van het cellichaam van welke axon is afkomstig van het axon?
- Wat is abnocious?
- Wat geeft embryologie aan over verschillende organismen?
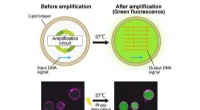
- Nieuwe DNA-amplificatiecapsule belooft veel voor de bestrijding van ziekten
- Wetenschappers gebruiken coöperatieve actie van een ligand-tegenionsysteem voor duurzame etherproductie

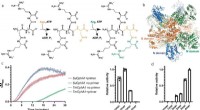
- De verrassende Zwitserse legermes-achtige functies van een krachtig enzym
- Linkse of rechtse moleculen helpen materiële structuren

- Nanokristallen worden beter als ze verdubbelen met MOF's

 Nieuwe benaderingen van het mysterie waarom ijs glad is
Nieuwe benaderingen van het mysterie waarom ijs glad is  Wat komt er vrij wanneer de chemische binding verbroken tussen tweede en derde fosfaat van een ATP -molecuul?
Wat komt er vrij wanneer de chemische binding verbroken tussen tweede en derde fosfaat van een ATP -molecuul?  Welke enkele steek van fel licht?
Welke enkele steek van fel licht?  Onderzoek toont aan dat de zware weerspatronen in China sinds 1960 drastisch veranderen
Onderzoek toont aan dat de zware weerspatronen in China sinds 1960 drastisch veranderen Cellulaire chirurgie uitvoeren met een laseraangedreven nanoblade
Cellulaire chirurgie uitvoeren met een laseraangedreven nanoblade Hoe vergemakkelijkt DNA -structuur replicatie?
Hoe vergemakkelijkt DNA -structuur replicatie?  Verschillen tussen huisdiertraining en dierenconditionering
Verschillen tussen huisdiertraining en dierenconditionering  Welk proces komt voor in een cellen mitochondria?
Welk proces komt voor in een cellen mitochondria?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

