
Wetenschap
Chemische reactiviteit begrijpen:factoren die atoominteracties beïnvloeden
1. Elektronenconfiguratie:
* Valentie-elektronen: De buitenste elektronen in een atoom worden valentie-elektronen genoemd. Deze elektronen zijn betrokken bij chemische binding. Atomen hebben de neiging te reageren om een stabiele elektronenconfiguratie te bereiken, meestal een volledige buitenste schil (octetregel).
* Elektronegativiteit: Dit is een maatstaf voor het vermogen van een atoom om elektronen in een binding aan te trekken. Atomen met een hoge elektronegativiteit hebben de neiging elektronen te winnen, terwijl atomen met een lage elektronegativiteit de neiging hebben elektronen te verliezen.
2. Nucleaire lading:
* Aantal protonen: Het aantal protonen in de kern bepaalt het atoomnummer en de sterkte van de positieve lading. Een hogere nucleaire lading trekt elektronen sterker aan.
3. Energieniveaus en orbitalen:
* Energieniveaus: Elektronen bezetten specifieke energieniveaus binnen een atoom. Atomen reageren om een lagere energietoestand te bereiken.
* Orbitalen: Elektronen bezetten specifieke orbitalen binnen energieniveaus. De vorm en oriëntatie van orbitalen beïnvloeden de binding.
4. Ionisatie-energie en elektronenaffiniteit:
* Ionisatie-energie: De energie die nodig is om een elektron uit een atoom te verwijderen. Atomen met een lage ionisatie-energie hebben de neiging elektronen te verliezen.
* Elektronenaffiniteit: De energieverandering wanneer een elektron wordt toegevoegd aan een neutraal atoom. Atomen met een hoge elektronenaffiniteit hebben de neiging elektronen te verkrijgen.
5. Soorten chemische bindingen:
* Ionische bindingen: Gevormd door de overdracht van elektronen tussen atomen, waardoor ionen met tegengestelde ladingen ontstaan. Deze bindingen komen meestal voor tussen atomen met een aanzienlijk verschillende elektronegativiteit.
* Covalente obligaties: Gevormd door het delen van elektronen tussen atomen. Deze bindingen komen meestal voor tussen atomen met een vergelijkbare elektronegativiteit.
* Metaalverbindingen: Komen voor tussen metaalatomen, waar elektronen door het metalen rooster worden gedelokaliseerd.
6. Andere factoren:
* Temperatuur: Een verhoogde temperatuur verhoogt vaak de snelheid van chemische reacties.
* Druk: Voor reacties waarbij gassen betrokken zijn, kan een verhoogde druk reacties bevorderen die minder gasmoleculen produceren.
* Aanwezigheid van katalysatoren: Katalysatoren versnellen chemische reacties zonder daarbij verbruikt te worden.
Samenvattend hangt de neiging van een atoom om te reageren af van zijn elektronenconfiguratie, nucleaire lading, energieniveaus en het potentieel om stabiele bindingen met andere atomen te vormen. Deze factoren bepalen hoe gemakkelijk een atoom elektronen kan winnen, verliezen of delen om een stabielere toestand te bereiken.
 AI for Earth:hoe NASA's kunstmatige intelligentie en open wetenschapsinspanningen de klimaatverandering bestrijden
AI for Earth:hoe NASA's kunstmatige intelligentie en open wetenschapsinspanningen de klimaatverandering bestrijden  Dier- en plantlevenscycli
Dier- en plantlevenscycli  NASA vindt kleine overblijfselen van tropische cycloon Owen
NASA vindt kleine overblijfselen van tropische cycloon Owen EPA-actie stimuleert het momentum om giftige chemicaliën voor altijd te verminderen
EPA-actie stimuleert het momentum om giftige chemicaliën voor altijd te verminderen Deepwater Horizon-olie heeft een dramatisch effect op de zintuiglijke vermogens van pijlstaartroggen
Deepwater Horizon-olie heeft een dramatisch effect op de zintuiglijke vermogens van pijlstaartroggen
Hoofdlijnen
- Waar bestaat de cel uit?
- Zijn de cellen van varen die u haploïde of diploïde ziet?
- Kunstmatig leven
- Hoe beïnvloedt menselijke activiteiten de groei van planten?
- Welke van de volgende soorten draagt een negatieve lading1 β -deeltje 2 γ -stralen 3 protonen 4 α -deeltje?
- Waarom worden nucleïnezuren in alle voedingsmiddelen aangetroffen?
- Studie:Net als een boom laten jaarringen de leeftijd van de kreeft zien
- Welk type metabolisme doet Archaea?
- Natuur, opvoeding of natuurkunde? Onderzoekers beantwoorden vragen over het gedrag van nematoden
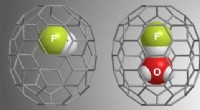
- Onderzoekers isoleren waterstoffluoride en water om zuuroplossing te begrijpen
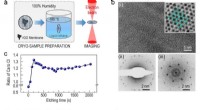
- Nieuw waargenomen eenwaardige calciumionen vertonen onverwachte metaalachtigheid en ferromagnetisme
- Nieuw buigbaar cementvrij beton kan mogelijk veiliger, duurzame en groenere infrastructuur

- Een betere magere aardappelchips ontwerpen
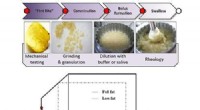
- Maakt het mogelijk om grotere 3D-geprinte objecten te maken met keramiek

 Wat gebeurt er als de Top Predator wordt verwijderd uit een ecosysteem?
Wat gebeurt er als de Top Predator wordt verwijderd uit een ecosysteem?  Hoe religie het vertrouwen in het vaderschap bevordert
Hoe religie het vertrouwen in het vaderschap bevordert  2 liter 0 een halve gallon?
2 liter 0 een halve gallon?  In welk seizoen komen stofstormen het meest voor?
In welk seizoen komen stofstormen het meest voor?  Hoe evolutie de meest efficiënte vleugelprofielen bouwt
Hoe evolutie de meest efficiënte vleugelprofielen bouwt  Nieuw deep learning-model gebruikt video om de embryonale ontwikkeling te meten
Nieuw deep learning-model gebruikt video om de embryonale ontwikkeling te meten  Waarom is elektriciteit zo'n nuttige bron in energie?
Waarom is elektriciteit zo'n nuttige bron in energie?  Welk instrument wordt meestal gebruikt om het volume van een vloeistof te meten?
Welk instrument wordt meestal gebruikt om het volume van een vloeistof te meten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

