
Wetenschap
Moleculaire geometrie van NH3 (ammoniak):een gedetailleerde uitleg
Dit is waarom:
* Centraal atoom: Stikstof (N)
* Aantal valentie-elektronen: Stikstof heeft 5 valentie-elektronen.
* Aantal verbindingsparen: Stikstof vormt 3 enkele bindingen met 3 waterstofatomen (H).
* Aantal alleenstaande paren: Stikstof heeft één eenzaam elektronenpaar.
VSEPR-theorie: De Valence Shell Electron Pair Repulsion-theorie voorspelt dat elektronenparen rond een centraal atoom zichzelf zullen rangschikken om afstoting te minimaliseren. Dit leidt tot het volgende:
* De 3 bindingsparen en 1 alleenstaand paar rond het stikstofatoom zullen zichzelf in een tetraëdrische vorm rangschikken.
*Het eenzame paar neemt echter meer ruimte in beslag dan de bindingsparen, waardoor de waterstofatomen dichter bij elkaar worden gedrukt.
* Dit resulteert in een vervormde tetraëdrische vorm, met name een trigonale piramide geometrie.
Visuele weergave: Stel je een piramide voor met een stikstofatoom aan de top en de drie waterstofatomen aan de basis. Het eenzame paar op de stikstof bevindt zich boven de basis van de piramide.
 Wat is stikstof het negatief of positieve ionen?
Wat is stikstof het negatief of positieve ionen?  Wat is de naam van ionische samengestelde mgso4?
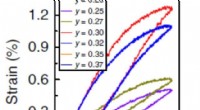
Wat is de naam van ionische samengestelde mgso4?  Berekeningsanalyse ontrafelt het complexe gedrag van een polymeer
Berekeningsanalyse ontrafelt het complexe gedrag van een polymeer Hoe verschilt de moderne atoomtheorie van de Daltons -theorie?
Hoe verschilt de moderne atoomtheorie van de Daltons -theorie?  Wat is de chemische formule van een ionische samengestelde aluminium en chloor?
Wat is de chemische formule van een ionische samengestelde aluminium en chloor?
 Septische systemen zijn een belangrijke bron van opkomende verontreinigingen in drinkwater
Septische systemen zijn een belangrijke bron van opkomende verontreinigingen in drinkwater NASA- en NOAA-satellieten volgen Alberto in het zuiden van de VS
NASA- en NOAA-satellieten volgen Alberto in het zuiden van de VS Uit onderzoek blijkt hoe de natuurbeschermingsboodschappen van Disney ons wild van hart hebben gehouden
Uit onderzoek blijkt hoe de natuurbeschermingsboodschappen van Disney ons wild van hart hebben gehouden  Is het planten van bomen om de klimaatverandering tegen te gaan 'complete onzin'?
Is het planten van bomen om de klimaatverandering tegen te gaan 'complete onzin'?  Heliumballonnen bieden goedkope vluchten naar de stratosfeer
Heliumballonnen bieden goedkope vluchten naar de stratosfeer
Hoofdlijnen
- Kan aminozuur ook ontwikkeld worden als pesticide tegen plantenvirussen?
- Wetenschappers vinden ontbrekende schakel om te begrijpen hoe planten vitamine C aanmaken
- Nieuw inzicht over hoe virussen gastheereiwitten in hun voordeel gebruiken
- In welk pH -niveau overleeft de meeste organismen?
- Wat had de grootste impact op de biologie in de 20e eeuw?
- Hoe beïnvloeden zowel genen als omgevingen eigenschappen?
- Wat kunt u een kern in cel vergelijken?
- Wat is de aanpassing van een ciliated cel?
- Waarom moet het menselijk lichaam grote macromoleculen verteren in kleine monomeren voordat het ze als energiebron kan gebruiken?
- Ingenieur-kliniekteam gebruikt actieve rimpels om synthetische transplantaten schoon te houden

- Nieuw keramisch materiaal kan de kosten van piëzo-elektrische apparaten verlagen
- Vegan spinzijde biedt duurzaam alternatief voor plastic voor eenmalig gebruik

- Met grafeen gewikkelde zeolietmembranen voor snelle waterstofscheiding

- Platform met hoge doorvoer maakt het in kaart brengen van activiteiten van opkomende kankergeneesmiddelen mogelijk

 Hoe werken droge chemische brandblussers?
Hoe werken droge chemische brandblussers?  Hoe een wetenschapsproject te doen op vingerafdrukken
Hoe een wetenschapsproject te doen op vingerafdrukken  Wordt Technetium gevonden in een samengestelde of pure elementaire vorm?
Wordt Technetium gevonden in een samengestelde of pure elementaire vorm?  Sneeuwvalpatronen kunnen aanwijzingen geven voor de Groenlandse ijskap
Sneeuwvalpatronen kunnen aanwijzingen geven voor de Groenlandse ijskap Microscopie plus AI staat gelijk aan snelle COVID-19-detectie:studie
Microscopie plus AI staat gelijk aan snelle COVID-19-detectie:studie Welke verbinding bevat alleen de elementen koolstofwaterstof en zuurstof?
Welke verbinding bevat alleen de elementen koolstofwaterstof en zuurstof?  Een geleider met een hoge temperatuur heeft waarschijnlijk high?
Een geleider met een hoge temperatuur heeft waarschijnlijk high?  Wat is een object dat banen groter wordt genoemd?
Wat is een object dat banen groter wordt genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

