
Wetenschap
Waarom HCl in tolueen niet blauw lakmoesrood wordt:oplosbaarheid en ionisatie begrijpen
* Tolueen is een niet-polair oplosmiddel: Tolueen is een koolwaterstof en de moleculen ervan zijn niet-polair.
* HCl is een polair molecuul: HCl is een polair molecuul, met een positieve lading op het waterstofatoom en een negatieve lading op het chlooratoom.
* "Like lost like op": Polaire moleculen hebben de neiging op te lossen in polaire oplosmiddelen, terwijl niet-polaire moleculen oplossen in niet-polaire oplosmiddelen.
Omdat tolueen niet-polair is, kan het de polaire HCl-moleculen niet effectief solvateren. Dit betekent dat HCl in tolueen niet dissocieert in H+ en Cl-ionen, zoals dat wel het geval zou zijn in een polair oplosmiddel zoals water.
Om lakmoespapier rood te laten worden, moet het in contact komen met H+-ionen. Omdat HCl in tolueen geen vrije H+-ionen produceert, blijft het lakmoespapier blauw.
 Studie verklaart wetenschap achter een van de nieuwste erkende wolken
Studie verklaart wetenschap achter een van de nieuwste erkende wolken Wat is de sfeer van Het tij stijgt en valt?
Wat is de sfeer van Het tij stijgt en valt?  Botsingsrisico en verlies van leefgebied:studie onderzoekt hoe windturbines in bossen bedreigde vleermuissoorten schaden
Botsingsrisico en verlies van leefgebied:studie onderzoekt hoe windturbines in bossen bedreigde vleermuissoorten schaden  Wat is een productiebos?
Wat is een productiebos?  Cyclonen en klimaatverandering:de stippen verbinden
Cyclonen en klimaatverandering:de stippen verbinden
Hoofdlijnen
- 'Vliegende vaccinator':kunnen genetisch gemanipuleerde muggen een nieuwe strategie tegen malaria bieden?
- Waarom stijgt je lichaamstemperatuur als je een virus hebt zoals griep?
- Een cel die een andere cel overspoelt?
- Type RNA dat het aminozuur naar Messenger Strand brengt?
- Kiemvrije broedeieren:een alternatief voor het gebruik van formaldehyde
- Wat is een belangrijke biologische gemeenschap die zich voordoet over een groot landgebied?
- Reageert hetzelfde organisme altijd op weg op stimulus?
- Seizoensregulatie in de biologische klok van de bonenbughersenen
- Wat zijn de subsystemen van het lichaam?
- Hoe u vlakglas perfect om hoeken buigt

- Katalysatoren voor een betere productie van biobrandstoffen

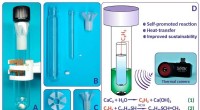
- Chemici vinden een efficiënte thermische camera uit om de kosten van chemisch onderzoek te verlagen
- Wiebelen en wiebelen:studie legt uit hoe organismen evolueren om bij verschillende temperaturen te leven

- Propionzuur:eigenschappen, productie en voedselveiligheid

 Oceaanalgen krijgen genade van virussen
Oceaanalgen krijgen genade van virussen Hoe wordt een circuit-aangedreven testlicht gebruikt?
Hoe wordt een circuit-aangedreven testlicht gebruikt?  Welke heeft de sterkste intermoleculaire kracht NH3 of H20?
Welke heeft de sterkste intermoleculaire kracht NH3 of H20?  Welke wetenschapper stelde voor dat cellen uit pre -bestaande cellen komen?
Welke wetenschapper stelde voor dat cellen uit pre -bestaande cellen komen?  Welk transport moet mogelijk energie -pass door celmembraan gebruiken?
Welk transport moet mogelijk energie -pass door celmembraan gebruiken?  Hoe ver zijn Scorpius en Orion?
Hoe ver zijn Scorpius en Orion?  Water omzetten in elektriciteit
Water omzetten in elektriciteit Hoe werkt ioniserende straling voor sterilixe -insecten?
Hoe werkt ioniserende straling voor sterilixe -insecten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

