
Wetenschap
Ethanol versus propanol:de moleculaire polariteit begrijpen
Polariteit is een maat voor de ongelijke verdeling van de elektronendichtheid binnen een molecuul. Hoe polairder een molecuul is, des te sterker interageert het met andere polaire moleculen (zoals water).
Dit is de reden waarom ethanol meer polair is:
* Structuur: Ethanol (CH3CH2OH) heeft een kleinere koolstofketen vergeleken met propanol (CH3CH2CH2OH).
* Hydroxylgroep: Beide moleculen bevatten een hydroxylgroep (-OH), die zeer polair is vanwege het elektronegativiteitsverschil tussen zuurstof en waterstof.
* Inductief effect: Door de kleinere koolstofketen in ethanol kan de polariteit van de hydroxylgroep een sterkere invloed hebben op het molecuul als geheel. De langere koolstofketen in propanol "verdunt" enigszins het effect van de hydroxylgroep.
Samengevat:
*De hydroxylgroep levert de belangrijkste bijdrage aan de polariteit.
* De kleinere koolstofketen in ethanol zorgt voor een sterkere invloed van de polariteit van de hydroxylgroep.
Daarom is ethanol polairder dan propanol.
 Waarom wordt zilvernitraat gebruikt in de chloridegrenstest?
Waarom wordt zilvernitraat gebruikt in de chloridegrenstest?  Wat is de chemische formule voor tin iv thiosulfaat?
Wat is de chemische formule voor tin iv thiosulfaat?  Aluminium hardheidsclassificatie
Aluminium hardheidsclassificatie  Nieuwe geleidende polymeerinkt opent voor de volgende generatie gedrukte elektronica
Nieuwe geleidende polymeerinkt opent voor de volgende generatie gedrukte elektronica Wat is een wetenschappelijk wetenschap van graad 8 aangedreven door vloeistoffen of gassen?
Wat is een wetenschappelijk wetenschap van graad 8 aangedreven door vloeistoffen of gassen?
 Uit onderzoek in Fiji blijkt dat het verwijderen van zeekomkommers problemen oplevert voor ondiepe kustwateren
Uit onderzoek in Fiji blijkt dat het verwijderen van zeekomkommers problemen oplevert voor ondiepe kustwateren Klimaatverandering vormt een onzekere toekomst voor de aquatische habitats van Indianas
Klimaatverandering vormt een onzekere toekomst voor de aquatische habitats van Indianas Organellen die betrokken zijn bij fotosynthese
Organellen die betrokken zijn bij fotosynthese  Fun Rainforest Science Experiments
Fun Rainforest Science Experiments De verdwijnende wateren van Tulare Lake:hoe het grote meer van Central Valley in Californië komt en gaat
De verdwijnende wateren van Tulare Lake:hoe het grote meer van Central Valley in Californië komt en gaat
Hoofdlijnen
- Hoe werkt het skelet met het ademhalingssysteem?
- Is hun geen limiet in hoe groot of klein een cel kan zijn?
- Wat omringt de kern en houdt deze in elkaar?
- Het onzichtbare zien:hoe vlinders wetenschappers kunnen helpen kanker op te sporen
- Wat is het oudste celtype?
- Leg de rol van X- en Y -chromosomen uit bij het bepalen van het geslacht?
- De enige essentiële organel van een cel?
- Waar is de buitenste celwand van een bacterie van gemaakt?
- Wat is de betekenis van Microbe Deinococcus radiodurans?
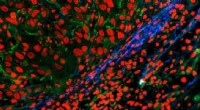
- Weefselvorming verlichten door fluorescentie
- Aluminiumrecyclingtechnologie gestimuleerd door kristallisatieonderzoek

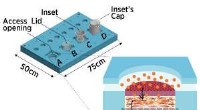
- Huid reconstrueren op een chip
- Metalen vijfledige ring verlegt de grenzen van aromaticiteit

- Technologie onthult voorheen niet-detecteerbare eiwitsignaleringsactiviteit bij diabetes, kanker

 Meer elektronische materialen geopend met nieuw metaal-organisch raamwerk
Meer elektronische materialen geopend met nieuw metaal-organisch raamwerk Wie heeft de wetenschappelijke eigendom van elektriciteit ontdekt?
Wie heeft de wetenschappelijke eigendom van elektriciteit ontdekt?  Onderzoekers ontdekken kristallijne zeolieten in nanobuisvorm
Onderzoekers ontdekken kristallijne zeolieten in nanobuisvorm Wat is een materiaal dat de energieoverdracht mogelijk maakt?
Wat is een materiaal dat de energieoverdracht mogelijk maakt?  Wat is de wind die uit zee blaast?
Wat is de wind die uit zee blaast?  In welke eenheid is het imperiaal gemeten snelheid?
In welke eenheid is het imperiaal gemeten snelheid?  Wat zijn de belangrijkste waterlichamen in de buurt van Tundra Biome?
Wat zijn de belangrijkste waterlichamen in de buurt van Tundra Biome?  Hoe de Accuplacer Math Test door te geven
Hoe de Accuplacer Math Test door te geven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

