
Wetenschap
Inzicht in de sterkere aantrekkingskracht tussen ijzer- en sulfide-ionen
1. Ladingsdichtheid:
* IJzerionen: IJzerionen hebben een hogere ladingsdichtheid dan zinkionen. Dit betekent dat de positieve lading geconcentreerd is over een kleiner gebied, wat leidt tot een sterkere elektrostatische aantrekkingskracht op het negatief geladen sulfide-ion.
* Zinkionen: Zinkionen hebben een grotere ionenstraal en een lagere ladingsdichtheid. Deze zwakkere ladingsdichtheid resulteert in een zwakkere elektrostatische aantrekking tot sulfide-ionen.
2. Elektronegativiteit:
* IJzer: IJzer is elektronegatiever dan zink. Dit betekent dat ijzer een sterkere aantrekkingskracht heeft op elektronen, waardoor het waarschijnlijker is dat het een sterke ionische binding vormt met het sulfide-ion.
3. Hard-zachte zuur-base-theorie:
* IJzer: IJzer wordt als een harder zuur beschouwd, terwijl sulfide een zachtere base is. Harde zuren hechten zich het liefst aan harde basen, en omgekeerd. Dit verklaart de sterkere aantrekkingskracht tussen ijzer en sulfide.
* Zink: Zink wordt als een zachter zuur beschouwd en de aantrekkingskracht ervan op de zachtere sulfidebase is zwakker in vergelijking met ijzer.
4. Roosterenergie:
* De roosterenergie, de energie die nodig is om de ionen in een vaste stof te scheiden, is hoger voor ijzersulfide (FeS) vergeleken met zinksulfide (ZnS). Dit duidt op een sterkere aantrekkingskracht tussen de ionen in ijzersulfide.
Samengevat:
De combinatie van een hogere ladingsdichtheid, sterkere elektronegativiteit en een betere match in de hard-zachte zuur-base-theorie leidt tot een sterkere aantrekkingskracht tussen ijzerionen en sulfide-ionen vergeleken met zinkionen. Dit is de reden waarom ijzersulfide stabieler is en gemakkelijker wordt gevormd dan zinksulfide.
Het is belangrijk op te merken dat dit een vereenvoudigde uitleg is. Andere factoren, zoals solvatatie-effecten en de aanwezigheid van andere liganden, kunnen ook de relatieve stabiliteit van deze verbindingen beïnvloeden.
 Atomen in de lucht:de samenstelling van onze atmosfeer begrijpen
Atomen in de lucht:de samenstelling van onze atmosfeer begrijpen  Als 2 mol natriumcarbonaat wordt gebruikt in de reactie, hoeveel gram chloride zal worden gevormd?
Als 2 mol natriumcarbonaat wordt gebruikt in de reactie, hoeveel gram chloride zal worden gevormd?  Gewoon een molecuul naar een biomolecuul klikken voor een andere functie
Gewoon een molecuul naar een biomolecuul klikken voor een andere functie Hoe zou 10 g heliumgas anders zijn dan in een verzegelde pot?
Hoe zou 10 g heliumgas anders zijn dan in een verzegelde pot?  Wat is de juiste naam voor samengestelde HCL03?
Wat is de juiste naam voor samengestelde HCL03?
Hoofdlijnen
- Welke organismen kunnen niet worden bekeken met behulp van de samengestelde microscoop?
- Schimmelreproductie:seksuele en aseksuele methoden uitgelegd
- Bacteriën hebben tastzin
- Lijst 10 enzymen die in het menselijk lichaam worden gevonden?
- Wat is een wetenschapper die in het water werkt?
- Hoe zal zalm overleven in een overstroomde toekomst?
- Hoe nemen cellen in voedingsstoffen op om te groeien en te verdelen de benodigde materialen?
- Wanneer beide soorten profiteren van de relatie die het wordt genoemd?
- De nakomelingen van een plant die aseksueel reproduceert?
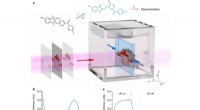
- Nieuwe chemie voor het regelen van het vloeistofvolume in volumetrische additieve productie
- Chemici waarschuwen voor onredelijke verspilling bij aanschaf van wetenschappelijke apparatuur

- Eerste flexibele geheugenapparaat dat ferro-elektrisch materiaal van oxide gebruikt

- Bouw een 3D-atoommodel:een stapsgewijze handleiding voor wetenschappelijke projecten
- Materiaal om de overgang naar schone waterstofbrandstof te helpen

 Waar worden eiwitten voor in planten gebruikt?
Waar worden eiwitten voor in planten gebruikt?  In welk continent zit Polynesië?
In welk continent zit Polynesië?  Hoe worden eiwitten gevormd door het concept van polymerisatie te gebruiken?
Hoe worden eiwitten gevormd door het concept van polymerisatie te gebruiken?  De kracht tussen een paar van 0,001 C ladingen is 200 n Wat de afstand van hen?
De kracht tussen een paar van 0,001 C ladingen is 200 n Wat de afstand van hen?  Is het korst een deel van de sfeer?
Is het korst een deel van de sfeer?  Wat zijn vragen en antwoorden over Uranus Neptunus?
Wat zijn vragen en antwoorden over Uranus Neptunus?  De voordelen van Simple Distillation
De voordelen van Simple Distillation Welk gas wordt uitgegeven als zuur reageert met een alkali?
Welk gas wordt uitgegeven als zuur reageert met een alkali?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

