
Wetenschap
Vorming van natrium-chloorbindingen:Ionische bindingen en keukenzout (NaCl) begrijpen
* Natrium (Na): Natrium heeft één elektron in de buitenste schil. Het wil dit elektron kwijtraken om een stabiele elektronenconfiguratie te bereiken zoals de edelgassen.
* Chloor (Cl): Chloor heeft zeven elektronen in de buitenste schil. Het wil één elektron winnen om een stabiele elektronenconfiguratie te bereiken, zoals de edelgassen.
De uitwisseling:
1. Natrium verliest een elektron: Het natriumatoom geeft zijn eenzame valentie-elektron op en wordt een positief geladen natriumion (Na+).
2. Chloor krijgt een elektron: Het chlooratoom accepteert het elektron van natrium en wordt een negatief geladen chloride-ion (Cl-).
3. Vorming van ionenbindingen: De tegengesteld geladen ionen (Na+ en Cl-) worden door elektrostatische krachten tot elkaar aangetrokken, waardoor een ionische binding ontstaat. Deze aantrekkingskracht is sterk en resulteert in de vorming van een kristalroosterstructuur in vast NaCl.
Resultaat:
Door de uitwisseling van een elektron tussen natrium en chloor ontstaat een stabiele verbinding, natriumchloride (NaCl). Deze verbinding is een witte, kristallijne vaste stof die algemeen bekend staat als keukenzout.
Samengevat:
* Het natriumatoom verliest een elektron en wordt een positief geladen ion (Na+).
* Chlooratoom krijgt een elektron en wordt een negatief geladen ion (Cl-).
* De tegengesteld geladen ionen trekken elkaar aan, vormen een ionische binding en creëren natriumchloride (NaCl).
 Wat is systeemdecompositie en onderlinge afhankelijkheid van subsystemen?
Wat is systeemdecompositie en onderlinge afhankelijkheid van subsystemen?  Is het scheuren van papier een chemische verandering?
Is het scheuren van papier een chemische verandering?  Hoe worden enzymen weergegeven in een chemische vergelijking?
Hoe worden enzymen weergegeven in een chemische vergelijking?  Het volgen van eiwitverwijdering kan leiden tot verbeterde therapieën
Het volgen van eiwitverwijdering kan leiden tot verbeterde therapieën Waar zijn koolstofatomen in fotosynthese die voor worden gebruikt?
Waar zijn koolstofatomen in fotosynthese die voor worden gebruikt?
 Als dat geen mensenhanden zijn in oude grotkunst... Wat zijn dat dan?
Als dat geen mensenhanden zijn in oude grotkunst... Wat zijn dat dan?  Vraag en antwoord:La Nina kan meer Atlantische stormen brengen, westelijke droogte
Vraag en antwoord:La Nina kan meer Atlantische stormen brengen, westelijke droogte Donkere vezels leggen de basis voor detectie van aardbevingen op lange afstand en het in kaart brengen van grondwater
Donkere vezels leggen de basis voor detectie van aardbevingen op lange afstand en het in kaart brengen van grondwater Grootschalige tornado-uitbraken die in frequentie toenemen, studie vondsten
Grootschalige tornado-uitbraken die in frequentie toenemen, studie vondsten Het vochtproces dat wordt vrijgelaten uit de bladerenbomen en planten in de lucht?
Het vochtproces dat wordt vrijgelaten uit de bladerenbomen en planten in de lucht?
Hoofdlijnen
- Wat komt binnen en verlaat de kern?
- Wat zijn beweeglijke processen?
- Wat is de interactie tussen twee verschillende soorten die nauw samenleven?
- Waarom extraheren we DNA?
- Onderzoek van 300 miljoen jaar oude ontlasting vindt vlees op het menu
- Moleculaire modellen versus andere modellen:belangrijkste verschillen verklaard
- De organellen die witte bloedcellen in staat stellen bacteriën in te nemen en te vernietigen zijn?
- Wat kunnen planten leren van algen?
- Welke organellen zijn talrijker in actieve cellen?
- Hoe water het substraat in het enzym helpt

- Het plastictekort oplossen met een nieuwe chemische katalysator
- Wetenschappers vinden potentiële ziektebestrijdende kernkoppen verborgen in bacteriën
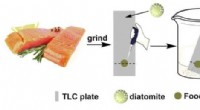
- Gefossiliseerde algen zijn veelbelovend voor verbeterde voedselveiligheidstesten
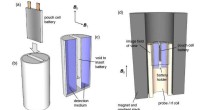
- Chemici ontwikkelen MRI-achtige techniek om te detecteren wat er aan de hand is met batterijen
 Nieuw proces recyclet overtollige koolstofdioxide efficiënter tot brandstof, studie vondsten
Nieuw proces recyclet overtollige koolstofdioxide efficiënter tot brandstof, studie vondsten Wat is de studie van krachten binnen de aarde die ervoor zorgen dat korst wordt geroepen?
Wat is de studie van krachten binnen de aarde die ervoor zorgen dat korst wordt geroepen?  Het paren van homologe chromosomen vóór nucleaire divisie gebeurt in welk type celdeling?
Het paren van homologe chromosomen vóór nucleaire divisie gebeurt in welk type celdeling?  Hoe bepaal je de toestand van een reactant en product?
Hoe bepaal je de toestand van een reactant en product?  Nieuwe vorm van op grafeen gebaseerd optisch materiaal ontwikkeld
Nieuwe vorm van op grafeen gebaseerd optisch materiaal ontwikkeld Engelennummer 155:de spirituele betekenis ervan ontcijferen
Engelennummer 155:de spirituele betekenis ervan ontcijferen  Hoeveel atomen heeft mg no3 2?
Hoeveel atomen heeft mg no3 2?  Sunrise III veilig gevonden op landingsplaats
Sunrise III veilig gevonden op landingsplaats
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

