
Wetenschap
Inzicht in de zwakke zuurgraad van waterstoffluoride (HF)
* Sterke waterstofbinding: Fluor is het meest elektronegatieve element, wat leidt tot een zeer polaire HF-binding. Deze sterke polariteit resulteert in uitgebreide waterstofbindingen tussen HF-moleculen in oplossing. De waterstofbruggen zijn zo sterk dat ze het proton (H+) effectief "vasthouden" en voorkomen dat het gemakkelijk in oplossing dissocieert.
* Klein formaat fluor: De kleine omvang van fluor zorgt voor een zeer nauwe interactie tussen het fluoratoom en het waterstofproton. Deze sterke interactie remt verder de dissociatie van het proton.
* Lage dissociatieconstante: De dissociatieconstante (Ka) van HF is aanzienlijk lager dan die van andere sterke zuren zoals HCl, HBr en HI. Deze lage Ka geeft aan dat slechts een klein deel van de HF-moleculen dissocieert in oplossing, wat de classificatie ervan als een zwak zuur verder ondersteunt.
In tegenstelling tot andere halogeniden (HCl, HBr, HI) verminderen de sterke waterstofbinding en de kleine omvang van fluor aanzienlijk de neiging van HF om protonen vrij te geven, waardoor het een zwak zuur wordt.
 Organische moleculen begrijpen:soorten, toepassingen en belang
Organische moleculen begrijpen:soorten, toepassingen en belang  Citroenzuur versus zoutoplosbaarheid:chemische oplossing begrijpen
Citroenzuur versus zoutoplosbaarheid:chemische oplossing begrijpen  Parodontitis:onderzoekers zoeken naar een nieuwe werkzame stof
Parodontitis:onderzoekers zoeken naar een nieuwe werkzame stof Welke producten worden gevormd uit de reactie van H2C2O4 H2O?
Welke producten worden gevormd uit de reactie van H2C2O4 H2O?  Waarom wordt goud geclassificeerd als een stof?
Waarom wordt goud geclassificeerd als een stof?
 Op het menu van een Brits restaurant:ecologische voetafdruk
Op het menu van een Brits restaurant:ecologische voetafdruk Afbeelding:Rook van bosbranden doorkruist VS op jetstream
Afbeelding:Rook van bosbranden doorkruist VS op jetstream Oude veranderingen langs de Hudson bieden een glimp van hoe ijskappen groeiden
Oude veranderingen langs de Hudson bieden een glimp van hoe ijskappen groeiden NASA onderzoekt de regen die is achtergelaten door ex-tropische cycloon Debbie
NASA onderzoekt de regen die is achtergelaten door ex-tropische cycloon Debbie Wat zijn de 10 beroepen die grondstoffen uit bossen en wilde dieren halen?
Wat zijn de 10 beroepen die grondstoffen uit bossen en wilde dieren halen?
Hoofdlijnen
- Wat gebruiken wetenschappers hulpmiddelen?
- Wat zijn organismen die voedsel moeten eten voor energie die wordt genoemd?
- Wat zijn de oorzaken van zulke overeenkomsten en verschillen in genen?
- Wat zijn cellen die geen afzonderlijke kern hebben genoemd?
- Betere mensen maken - Het huwelijk tussen mens en machine
- Van welke cellen delen de plant in staat om voedsel uit zonlicht te produceren?
- Hoe zijn RNA en DNA hetzelfde?
- Waarom zijn ontleders weggelaten uit bijna alle diagrammen voedselketens en -wB's?
- Wat is ATP en waarom het belangrijk is voor cellen?
- Suiker snel oplossen:eenvoudige tips voor snellere oplosbaarheid

- Moderne simulaties kunnen MRI's verbeteren
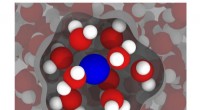
- Een nieuwe benadering van zonnecellen zappen

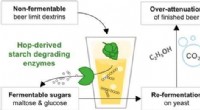
- Hoppig bier zonder ontploffende flessen en te veel alcohol
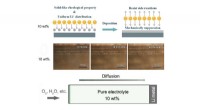
- Hydrofoob silica-colloïde-elektrolyt is veelbelovend voor veiligere lithium-zuurstofbatterijen
 Vergelijken en contrasteren met een gematigd bioom en een Taiga Biome
Vergelijken en contrasteren met een gematigd bioom en een Taiga Biome Wordt de samenstelling van een ionische verbinding gevormd door twee of meer niet-metalen elementen?
Wordt de samenstelling van een ionische verbinding gevormd door twee of meer niet-metalen elementen?  Wat is een andere naam voor de European Mountain Ash?
Wat is een andere naam voor de European Mountain Ash?  Wat is brandende zon?
Wat is brandende zon?  Wat zijn twee voorbeelden van verandering die niet door energie worden veroorzaakt en uitlegt?
Wat zijn twee voorbeelden van verandering die niet door energie worden veroorzaakt en uitlegt?  Wat betekent het woord grond in de wetenschap?
Wat betekent het woord grond in de wetenschap?  Waarom is de verklaringsnelheid van het licht van 300 miljoen mijl per seconde niet altijd correct?
Waarom is de verklaringsnelheid van het licht van 300 miljoen mijl per seconde niet altijd correct?  Hoe verschillende stadia van de aarde werden gevormd?
Hoe verschillende stadia van de aarde werden gevormd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

