
Wetenschap
Polariteit van NCl3-obligaties:chemische bindingen begrijpen
* Elektronegativiteit: Stikstof (N) heeft een elektronegativiteit van 3,04, terwijl chloor (Cl) een elektronegativiteit van 3,16 heeft. Dit verschil in elektronegativiteit, hoewel klein, creëert een dipoolmoment binnen elke N-Cl-binding.
* Dipoolmoment: Het chlooratoom trekt de gedeelde elektronen in de binding sterker aan dan het stikstofatoom. Hierdoor ontstaat een gedeeltelijk negatieve lading (δ-) op het chlooratoom en een gedeeltelijk positieve lading (δ+) op het stikstofatoom.
* Polaire covalente binding: Vanwege de ongelijke verdeling van elektronen en het resulterende dipoolmoment worden de N-Cl-bindingen in NCl3 beschouwd als polaire covalente bindingen.
Belangrijke opmerking: Terwijl de individuele bindingen in NCl3 polair zijn, is het totale molecuul zelf polair . Dit komt omdat de moleculaire geometrie van NCl3 trigonaal piramidaal is, wat leidt tot een netto dipoolmoment over het molecuul.
 Planetaire botsing die de maan vormde, maakte het leven op aarde mogelijk
Planetaire botsing die de maan vormde, maakte het leven op aarde mogelijk Welke natuurlijke hulpbronnen lopen in gevaar?
Welke natuurlijke hulpbronnen lopen in gevaar?  Wat gebeurt er als de plant in water wordt gestopt?
Wat gebeurt er als de plant in water wordt gestopt?  Bossen vallen uiteen in de tropen, maar komen elders samen. Dit is wat het betekent voor dieren in het wild en het klimaat
Bossen vallen uiteen in de tropen, maar komen elders samen. Dit is wat het betekent voor dieren in het wild en het klimaat  Terwijl Europa hard praat over het klimaat, gegevens laten zien dat de uitstoot is gestegen
Terwijl Europa hard praat over het klimaat, gegevens laten zien dat de uitstoot is gestegen
Hoofdlijnen
- Hoe evolutie werkt
- Welke activiteit kan een wetenschapper doen als onderdeel van het wetenschappelijke proces?
- Welk deel van een streng -DNA vertelt de cel wat eiwit moet maken?
- Wat is de vloeistof in cel?
- Hoe is de stikstofbasissequentie van een gen gerelateerd aan structuureiwit?
- Wat betekent witte bloedcellen?
- Wanneer vindt in bacterie celdeling plaats?
- Uit onderzoek blijkt hoe cellen ‘vuilniszakken’ vormen voor het recyclen van afval
- Wat doet Mitchochondria?
- Een onderzoek naar de instabiliteit van het rozenvenster

- Hoe werkt gekkotape?

- Forensische boekhouding kan toekomstige voedselfraude voorspellen

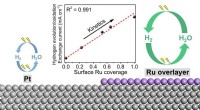
- Nieuwe mechanismen voor verbetering van de activiteit van bimetaalkatalysatoren voor waterstofopwekking en brandstofcellen
- Wetenschappers verduidelijken aspect van interacties tussen vaste stoffen en vloeistoffen in dunne film

 Hoe noem je moleculen die de meeste celfunctie uitvoeren?
Hoe noem je moleculen die de meeste celfunctie uitvoeren?  Wat zijn twee belangrijke geologische kenmerken in de buurt van een plaatgrens waar subductie plaatsvindt?
Wat zijn twee belangrijke geologische kenmerken in de buurt van een plaatgrens waar subductie plaatsvindt?  Foto's van koningsgetijden wereldwijd tonen risico's van klimaatverandering
Foto's van koningsgetijden wereldwijd tonen risico's van klimaatverandering Wat is het proces dat zich in de kern voordoet om zoveel energie te produceren?
Wat is het proces dat zich in de kern voordoet om zoveel energie te produceren?  Zuurstof- en stikstofbinding:ionisch versus covalent
Zuurstof- en stikstofbinding:ionisch versus covalent  Wat is de formule voor aluminium nitriet?
Wat is de formule voor aluminium nitriet?  Zijn de mineralen gedolven in Noord -Kaap hernieuwbaar?
Zijn de mineralen gedolven in Noord -Kaap hernieuwbaar?  Een nieuw materiaal gemaakt van koolstofnanobuisjes kan elektriciteit opwekken door energie uit de omgeving te halen
Een nieuw materiaal gemaakt van koolstofnanobuisjes kan elektriciteit opwekken door energie uit de omgeving te halen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

