
Wetenschap
Covalente obligaties begrijpen:eigenschappen, sterkte en richtingsgevoeligheid
1. Sterke hechtsterkte: Covalente bindingen zijn over het algemeen sterk, wat betekent dat ze veel energie nodig hebben om te breken. Dit komt omdat de gedeelde elektronen stevig tussen de gebonden atomen worden vastgehouden, wat resulteert in een stabiele en relatief lage energietoestand.
2. Directionele aard: Covalente bindingen zijn directioneel, wat betekent dat ze zich onder specifieke hoeken tussen de gebonden atomen vormen. Dit komt door de gelokaliseerde aard van de gedeelde elektronenparen, die specifieke gebieden in de ruimte bezetten.
3. Variabele bindingslengtes: De afstand tussen de kernen van twee covalent gebonden atomen, bekend als bindingslengte, kan variëren afhankelijk van de betrokken atomen en het type covalente binding.
4. Lage smelt- en kookpunten: Covalente verbindingen hebben over het algemeen lagere smelt- en kookpunten vergeleken met ionische verbindingen. Dit komt omdat de krachten die de moleculen bij elkaar houden zwakker zijn dan de elektrostatische krachten tussen ionen in ionische verbindingen.
5. Slechte elektrische geleidbaarheid: Covalente verbindingen zijn doorgaans slechte geleiders van elektriciteit in zowel vaste als vloeibare toestand. Dit komt omdat de elektronen stevig gebonden zijn binnen de gedeelde orbitalen en niet vrij kunnen bewegen. Er zijn echter uitzonderingen, zoals grafiet, dat een goede elektrische geleidbaarheid vertoont vanwege de gedelokaliseerde elektronen.
6. Onoplosbaar in water: De meeste covalente verbindingen zijn niet oplosbaar in water. Dit komt omdat water een polair oplosmiddel is en covalente verbindingen doorgaans niet-polair zijn, wat tot beperkte interacties leidt.
7. Vormen vaak moleculaire vaste stoffen: Covalente verbindingen vormen vaak moleculaire vaste stoffen, waarbij de moleculen bij elkaar worden gehouden door zwakke intermoleculaire krachten, zoals Van der Waals-krachten, waterstofbruggen of dipool-dipool-interacties. Deze krachten zijn zwakker dan de covalente bindingen in de moleculen, wat resulteert in de bovengenoemde lagere smelt- en kookpunten.
8. Verschillende toestanden van materie: Covalente verbindingen kunnen in alle drie de toestanden van de materie voorkomen:vast, vloeibaar en gas. Dit komt door het brede scala aan intermoleculaire krachten die tussen moleculen kunnen bestaan, die hun smelt- en kookpunten beïnvloeden.
9. Verscheidenheid aan fysieke eigenschappen: Covalente verbindingen vertonen een breed scala aan fysische eigenschappen, waaronder kleur, hardheid en dichtheid. Deze eigenschappen worden beïnvloed door de specifieke betrokken atomen, het aantal en de soorten covalente bindingen en de rangschikking van de atomen binnen het molecuul.
Het is belangrijk om te onthouden dat deze eigenschappen algemene trends zijn en dat er uitzonderingen zijn. Deze fysieke kenmerken helpen ons echter de aard van covalente bindingen en de eigenschappen van verbindingen gevormd door deze bindingen te begrijpen.
Hoofdlijnen
- Wat is het pad voor voedsel in het spijsverteringsstelsel van konijnen?
- Onderzoek toont verbeterde wortelgroei aan in met radiocesium verontreinigde grond
- De griezelige vraag van de vogelgriep:hoe miljoenen pluimvee te doden
- Wat transporteert eiwitten en synthese -lipiden?
- Wat is de werking van cacl2 om een bacteriële cel competent te maken?
- Your Brain On: An All Nighter
- Wat gebeurt er wanneer moleculen ATP de andere van de ene kant van een membraan pompen?
- Uit onderzoek blijkt dat Beluga-walvissen veranderen wat ze eten als gevolg van de klimaatverandering
- Welke structuren moeten organismen die geen celwand missen, ondersteuning bieden?
- Engineering van een polymeernetwerk om op verzoek als actieve camouflage te fungeren

- Kunstmatige materialen reconstrueren bruinvissen echolocatie
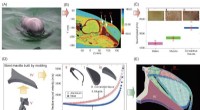
- Realtime atomaire beweging volgen tussen kristalkorrels in metalen

- Door spanning toe te voegen, onderzoekers verbeteren metaalglas

- Nieuw systeem maakt snel, antibioticabehandelingen op maat mogelijk

 Topsport wordt een platform om de transgemeenschap te targeten
Topsport wordt een platform om de transgemeenschap te targeten Late Tias-veranderingen terrestrische ecosystemen
Late Tias-veranderingen terrestrische ecosystemen Miljoenen O2, SoftBank-klanten getroffen door een storing
Miljoenen O2, SoftBank-klanten getroffen door een storing Welke vruchten groeien in de noordoostelijke regio?
Welke vruchten groeien in de noordoostelijke regio?  Donkere vezels leggen de basis voor detectie van aardbevingen op lange afstand en het in kaart brengen van grondwater
Donkere vezels leggen de basis voor detectie van aardbevingen op lange afstand en het in kaart brengen van grondwater Waar in de lucht is Melkweg gelokaliseerd?
Waar in de lucht is Melkweg gelokaliseerd?  Wat is het bijproduct van sucrose?
Wat is het bijproduct van sucrose?  CoH2O6SO4 decoderen:waarom deze chemische formule niet bestaat
CoH2O6SO4 decoderen:waarom deze chemische formule niet bestaat
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


