
Wetenschap
Inzicht in de aantrekkingskracht van water op natriumchloride (zout)
* Polariteit: Watermoleculen zijn polair, wat betekent dat ze een positief en negatief uiteinde hebben vanwege de ongelijke verdeling van elektronen. Het zuurstofatoom is enigszins negatief, terwijl de waterstofatomen enigszins positief zijn.
* Ionische binding: Natriumchloride is een ionische verbinding. Dit betekent dat het wordt gevormd door de elektrostatische aantrekkingskracht tussen positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-).
* Attractie: De positieve uiteinden van watermoleculen worden aangetrokken door de negatief geladen chloride-ionen, terwijl de negatieve uiteinden van watermoleculen worden aangetrokken door de positief geladen natriumionen. Deze aantrekkingskracht wordt elektrostatische aantrekkingskracht genoemd .
* Hydratatieschaal: Watermoleculen omringen de ionen en vormen een hydratatieschil. Deze schil isoleert de ionen effectief van elkaar, waardoor de ionische bindingen worden verzwakt en het zout in water kan oplossen.
Kort gezegd zorgt de polaire aard van watermoleculen ervoor dat ze kunnen interageren met de geladen ionen van natriumchloride, waardoor ze effectief uit elkaar worden getrokken en het zout wordt opgelost.
Hier zijn enkele aanvullende punten:
* Energie: Het proces waarbij zout in water wordt opgelost, is een endotherm proces , wat betekent dat het energie vereist. Deze energie komt uit het verbreken van de ionische bindingen in het zoutkristal en de vorming van nieuwe bindingen tussen watermoleculen en ionen.
* Oplosbaarheid: De oplosbaarheid van natriumchloride in water is relatief hoog, wat betekent dat een grote hoeveelheid zout in een bepaalde hoeveelheid water kan oplossen. Dit komt door de sterke aantrekkingskracht tussen watermoleculen en de ionen.
Over het geheel genomen is de aantrekkingskracht tussen watermoleculen en natriumchloride een sleutelfactor bij het oplossen van zout in water, een proces dat essentieel is voor veel biologische en chemische processen.
 Wat is de totale omgeving of alle omstandigheden die het leven en de groei van levende wezens beïnvloeden?
Wat is de totale omgeving of alle omstandigheden die het leven en de groei van levende wezens beïnvloeden?  Kan recycling slecht zijn voor het milieu?
Kan recycling slecht zijn voor het milieu?  Onder druk:hoe kamgelei zich heeft aangepast aan het leven op de bodem van de oceaan
Onder druk:hoe kamgelei zich heeft aangepast aan het leven op de bodem van de oceaan  Wat is de studie van dieren in hun natuurlijke omgeving?
Wat is de studie van dieren in hun natuurlijke omgeving?  Het is officieel:de afgelopen vijf jaar waren de warmste ooit gemeten
Het is officieel:de afgelopen vijf jaar waren de warmste ooit gemeten
Hoofdlijnen
- Hoe het ademhalingssysteem de homeostase handhaaft:zuurstof-, CO₂- en pH-regulering
- Wat betekent genetisch veranderd organisme?
- Het reconstrueren van fylogenieën door relaties af te leiden op basis van overeenkomsten die zijn afgeleid van een gemeenschappelijke voorouder zonder te overwegen dat de sterkte van karakter wordt genoemd?
- Bedoelden ze dat? Ongeval en opzet in een octopussentuin
- Wat produceren gistcellen door fermentatie in anaërobe ademhaling?
- Wat zijn de theorieën over erfenis vóór Mendel?
- Hoe is homoseksualiteit geëvolueerd? Er zou een aanwijzing in onze genen kunnen zitten
- Waarom is biotransformatie belangrijk?
- Wat is de opstelling van onderdelen in een organisme?
- Mengregels voor 3D-printbot
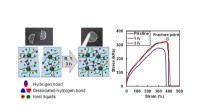
- De toekomst van elektronische apparaten:sterke en zelfherstellende iongels
- 3D-printen en maanstof:een astronautenkit voor toekomstige ruimteverkenning?

- Chemicaliënvrij, goedkope opbergzakken voor gewassen die voedsel langer bewaren nu in de handel verkrijgbaar

- Hoe temperatuur de vochtigheid beïnvloedt:een diepe duik in vocht, dauwpunt en verdamping

 Welke producten worden gevormd uit de reactie van H2C2O4 H2O?
Welke producten worden gevormd uit de reactie van H2C2O4 H2O?  Wat zijn de gevaren voor stralende energie?
Wat zijn de gevaren voor stralende energie?  Wat definieert de vorm van een cel?
Wat definieert de vorm van een cel?  Hoe krijgen cellen energie van koolhydraten en lipiden?
Hoe krijgen cellen energie van koolhydraten en lipiden?  Hoe veranderen genomen van soorten?
Hoe veranderen genomen van soorten?  Hoe weet hoe snel licht reist?
Hoe weet hoe snel licht reist?  Kunstmatige intelligentie verbetert biomedische beeldvorming
Kunstmatige intelligentie verbetert biomedische beeldvorming Simulaties tonen aan dat magnetisch veld 10 keer sneller kan veranderen dan eerder werd gedacht
Simulaties tonen aan dat magnetisch veld 10 keer sneller kan veranderen dan eerder werd gedacht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

