
Wetenschap
Identificatie van het beperkende reagens bij chemische reacties:een uitgebreide gids
Zo bepaalt u het beperkende reagens:
1. Schrijf een uitgebalanceerde chemische vergelijking: Dit toont de stoichiometrische verhoudingen van reactanten en producten.
2. Bereken het aantal mol van elke reactant: Gebruik de gegeven massa's en molmassa's.
3. Bepaal de molverhouding van de reactanten: Vergelijk de berekende mollen van elke reactant met de stoichiometrische coëfficiënten in de uitgebalanceerde vergelijking.
4. Identificeer het beperkende reagens: De reactant met de kleinste molverhouding ten opzichte van de coëfficiënt in de uitgebalanceerde vergelijking is het beperkende reagens.
Voorbeeld:
Beschouw de reactie:
2 H₂ (g) + O₂ (g) → 2 H₂O (l)
Laten we zeggen dat we:
* 4 gram H₂
* 16 gram O₂
1. Uitgebalanceerde vergelijking: Al gegeven.
2. Molen reactanten:
* H₂:4 g / 2 g/mol =2 mol
* O₂:16 g / 32 g/mol =0,5 mol
3. Molverhouding:
* H₂:2 mol / 2 =1
* O₂:0,5 mol / 1 =0,5
4. Beperkingsreagens: O₂ heeft de kleinere molverhouding (0,5) vergeleken met de coëfficiënt in de uitgebalanceerde vergelijking (1). Daarom is O₂ het beperkende reagens .
Belangrijke opmerking: Het beperkende reagens bepaalt de theoretische opbrengst van het product, wat de maximale hoeveelheid product is die kan worden gevormd.
 Aardbevingen verplaatsen zich naar het noordoosten in het Midland Basin van Texas, ontdekken wetenschappers
Aardbevingen verplaatsen zich naar het noordoosten in het Midland Basin van Texas, ontdekken wetenschappers  De aardbeving in Kaikoura kan ertoe leiden dat de modellen voor aardbevingsgevaar internationaal worden heroverwogen
De aardbeving in Kaikoura kan ertoe leiden dat de modellen voor aardbevingsgevaar internationaal worden heroverwogen Wat is wetenschappelijk ontwerp?
Wat is wetenschappelijk ontwerp?  Nieuw voorspellingssysteem waarschuwt inwoners van New Delhi over ongezonde lucht
Nieuw voorspellingssysteem waarschuwt inwoners van New Delhi over ongezonde lucht Infrarood NASA-beeld onthult de kracht van orkaan Fabios
Infrarood NASA-beeld onthult de kracht van orkaan Fabios
Hoofdlijnen
- Wat is een erosie?
- Bioloog ontdekt wat misschien wel de 'kieskeurigste' partners ter wereld zijn
- Welke cellen in uw lichaam kunnen hun vorm veranderen?
- Welke volgende kenmerken kunnen worden gebruikt om een organisme in een taxonomisch domein te classificeren?
- Een levende subeenheid van mensen?
- Een relatie waarin een organisme een ander organisme doodt en eet?
- Wat voor soort aseksuele reproductie omvat de groei van een klein organisme dat zich afbreekt van ouder om een ander volwassen organisme te produceren?
- Welke twee basistypen cellen vormen alle levende wezens?
- Wat is een Hullocigen?
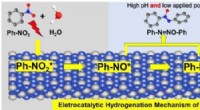
- Hydrogeneringsregeling van nitrobenzeen in elektrokatalytische processen gerealiseerd
- Boeiende klassikale activiteiten voor het onderwijzen van diffusie en osmose

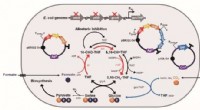
- Gemanipuleerde E. coli met mierenzuur en CO2 als een C1-raffinaderijplatformstam
- Hoge efficiëntie, goedkope katalysator voor waterelektrolyse

- Op jacht naar giftige stoffen in slib

 Wat zijn de vergelijkbare eigenschappen van zilveren silicium en zwavel?
Wat zijn de vergelijkbare eigenschappen van zilveren silicium en zwavel?  Waarom produceren citrusvruchten elektriciteit?
Waarom produceren citrusvruchten elektriciteit?  Geknepen licht doet de spiegels van Maagd trillen
Geknepen licht doet de spiegels van Maagd trillen Veelbelovend materiaal kan leiden tot snellere, goedkoper computergeheugen
Veelbelovend materiaal kan leiden tot snellere, goedkoper computergeheugen Tesla-aandeel daalt dichter bij pre-Musk-tweetniveau
Tesla-aandeel daalt dichter bij pre-Musk-tweetniveau Eerste bewijs voor een ongewone aangeboren pathologie bij holenberen
Eerste bewijs voor een ongewone aangeboren pathologie bij holenberen Hoeveel helderder is een supernova dan Nova?
Hoeveel helderder is een supernova dan Nova?  Een derde van de migranten- en vluchtelingenvrouwen krijgt te maken met huiselijk geweld, groot onderzoek onthult
Een derde van de migranten- en vluchtelingenvrouwen krijgt te maken met huiselijk geweld, groot onderzoek onthult
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

