
Wetenschap
Wat zijn de vier krachten die werken op aminozuren die in water worden geplaatst?
1. Waterstofbinding:
* Beschrijving: Aminozuren hebben functionele groepen zoals amine (-NH2) en carboxyl (-COOH) groepen, die waterstofbruggen kunnen vormen met watermoleculen. Dit is de primaire kracht die verantwoordelijk is voor de oplosbaarheid van aminozuren.
2. Elektrostatische interacties (ionische krachten):
* Beschrijving: De geladen groepen in aminozuren, zoals de amino- en carboxylgroepen bij de termini en de zijketens van sommige aminozuren (bijv. Lysine, arginine, glutaminezuur, asparaginezuur), kunnen interageren met watermoleculen door electrostatische interacties.
3. Van der Waals Forces:
* Beschrijving: Dit zijn zwakke aantrekkelijke krachten op korte afstand die optreden tussen alle moleculen, inclusief water en de niet-polaire delen van aminozuren. Ze dragen bij aan de algehele interacties, maar zijn minder significant dan waterstofbinding of elektrostatische krachten.
4. Hydrofobe interacties:
* Beschrijving: Niet-polaire zijketens van aminozuren hebben de neiging om samen te clusteren in water om hun contact met de polaire watermoleculen te minimaliseren. Dit wordt aangedreven door het entropische voordeel van watermoleculen die met elkaar inwerken, wat gunstiger is dan interactie met de hydrofobe zijketens.
5. Dipool-dipool interacties:
* Beschrijving: Hoewel vaak gegroepeerd onder van der Waals -krachten, worden deze interacties veroorzaakt door de permanente dipolen in polaire moleculen zoals water. Dit is belangrijk omdat de polaire aard van watermoleculen cruciaal is voor het oplossen van de polaire delen van aminozuren.
Sleutelpunt: Het samenspel van deze krachten, met name waterstofbinding, hydrofobe interacties en elektrostatische interacties, bepaalt de oplosbaarheid, conformatie en interacties van aminozuren in waterige omgevingen.
 Wat is de wet van behoud of aanklacht?
Wat is de wet van behoud of aanklacht?  Nieuwe gegevens over bodemvocht en temperatuur helpen levensbedreigende Indiase moessonregens te voorspellen
Nieuwe gegevens over bodemvocht en temperatuur helpen levensbedreigende Indiase moessonregens te voorspellen Levensbubbels uit het verleden:kleine zuurstofbelletjes kwamen 1,6 miljard jaar geleden vast te zitten
Levensbubbels uit het verleden:kleine zuurstofbelletjes kwamen 1,6 miljard jaar geleden vast te zitten Wat groeit een plant in de richting van licht dat wordt weergegeven?
Wat groeit een plant in de richting van licht dat wordt weergegeven?  Onderzoek toont aan dat droge lucht drijft over het hoofd gezien veranderingen in hoe planten drinken en ademen
Onderzoek toont aan dat droge lucht drijft over het hoofd gezien veranderingen in hoe planten drinken en ademen
Hoofdlijnen
- Wat is osmose een soort?
- Een soort bacteriën die de lactose van de melksuiker verteren?
- Welk type organisme zou in de meeste ecosystemen het minst overvloedig aanwezig zijn?
- Ribosoom endoplasmatisch reticulum en Golgi zijn delen van de cel genaamd wat?
- Wat beschrijft een in vivo experiment?
- Hoe multitasken werkt
- Welk organisme zou meestal op het 4e trofische niveau zijn?
- Tot welk lichaamssysteem behoort het hoornvlies?
- Welke pH- en wateractiviteitsniveaus groeien bacteriën?
- Alternatief cement met lage ecologische voetafdruk ontwikkeld
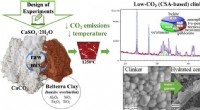
- Ontwikkeling van elektrodemateriaal dat de efficiëntie van zoutgehaltegradiëntenergie verbetert

- Suikers synthetiseren:scheikundigen ontwikkelen methode om de opbouw van koolhydraten te vereenvoudigen
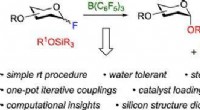
- De toekomst van biobrandstoffen in het donker

- Geïnspireerd door slakken, onderzoekers bedenken een omkeerbare lijm die sterk genoeg is om een persoon vast te houden

 Hoe Europa's CHEOPS-satelliet de jacht op exoplaneten zal verbeteren
Hoe Europa's CHEOPS-satelliet de jacht op exoplaneten zal verbeteren Verschil tussen kwarts en calciet
Verschil tussen kwarts en calciet  Nieuw bewijs van LHC toont aan dat pentaquark een molecuulachtige structuur heeft
Nieuw bewijs van LHC toont aan dat pentaquark een molecuulachtige structuur heeft Welke componenten maken energie?
Welke componenten maken energie?  Waar is hoeksnelheid gemeten?
Waar is hoeksnelheid gemeten?  Hoeveel chlooratomen zijn er in één molecuul PCL5?
Hoeveel chlooratomen zijn er in één molecuul PCL5?  Nano-inzichten kunnen leiden tot verbeterde kernreactoren:onderzoekers onderzoeken het zelfgenezend vermogen van sommige materialen
Nano-inzichten kunnen leiden tot verbeterde kernreactoren:onderzoekers onderzoeken het zelfgenezend vermogen van sommige materialen Kun je betrouwbaarheid beoordelen op basis van uiterlijk? Nieuw onderzoek zegt nee
Kun je betrouwbaarheid beoordelen op basis van uiterlijk? Nieuw onderzoek zegt nee
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

