
Wetenschap
Wat is altijd waar aan de temperatuur van een stof tijdens faseverandering?
Dit is waarom:
* Energie wordt gebruikt om bindingen te breken of te vormen: Tijdens een faseverandering (zoals smeltend ijs of kokend water), verhoogt de energie die wordt toegevoegd of verwijderd niet de kinetische energie van de moleculen (wat zou resulteren in een temperatuurstijging). In plaats daarvan wordt het gebruikt om de bindingen tussen moleculen te breken of te vormen, waardoor de toestand van materie is veranderd.
* latente hitte: De energie die wordt geabsorbeerd of afgegeven tijdens een faseverandering wordt latente warmte genoemd. Deze energie is "verborgen" omdat het niet resulteert in een temperatuurverandering, maar eerder een verandering in de toestand van de stof.
Voorbeeld:
Wanneer u ijs verwarmt, stijgt de temperatuur totdat deze 0 ° C (32 ° F) bereikt. Op dit punt begint het ijs te smelten. Hoewel je warmte blijft toevoegen, blijft de temperatuur op 0 ° C totdat al het ijs is gesmolten. De energie wordt gebruikt om de bindingen tussen de watermoleculen in het ijs te verbreken en ze in vloeibaar water te transformeren.
 Hoe scheid je ijzervullingen van babypoeder?
Hoe scheid je ijzervullingen van babypoeder?  Alle chemische en fysische veranderingen die plaatsvinden in het lichaam verwijzen naar?
Alle chemische en fysische veranderingen die plaatsvinden in het lichaam verwijzen naar?  Hoe een model van de neon te maken Atom
Hoe een model van de neon te maken Atom Studie voorspelt reactie van hartcellen op afnemende zuurstof
Studie voorspelt reactie van hartcellen op afnemende zuurstof IJzer II-verbindingen vormen een donkergroen neerslag wanneer natriumhydroxide wordt toegevoegd Waarom staat de bocht oranje bruin?
IJzer II-verbindingen vormen een donkergroen neerslag wanneer natriumhydroxide wordt toegevoegd Waarom staat de bocht oranje bruin?
Hoofdlijnen
- Een mogelijke manier om TR4-schimmelresistentie te verlenen aan Cavendish-bananen
- Wat is de naam van een georganiseerde groepscellen die samenwerken?
- Experimenten met verwarmde percelen laten een verband zien tussen warmere vroege winters en lagere oogstopbrengsten
- Een aanpassing om het oppervlak van een deelcel te vergroten die betrokken is bij cellulaire ademhaling?
- Een smakelijke wat trekt hongerige dieren aan die de plant kunnen helpen zijn zaden te verspreiden?
- Hoe kan het leven anders zijn als cellen actief transport moesten gebruiken, elke stof verplaatsen?
- Wat voor redenering wordt meestal gebruikt om hypothesen te vormen?
- Het ontsluiten van de geheimen van interacties tussen planten en elektromagnetische velden:een uitgebreid overzicht
- Waar komen de verschillende fasen van fotosynthese voor in cel?
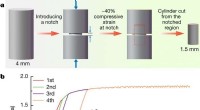
- Verjongend metaalglas om breuk te voorkomen
- Onderzoekers ontwikkelen sterkere microben om de bioproductie van brandstoffen te verbeteren, Chemicaliën
- Stralingsweerstand testen zonder een kernreactor te gebruiken

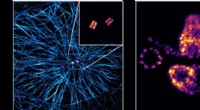
- Vooruitgang in superresolutiemicroscopie
- Ingenieurs produceren op additieve wijze elektriciteitspalen van biologisch afgeleide en gerecyclede materialen

 Hoe ver is Makemake van de aarde in mijlen of km?
Hoe ver is Makemake van de aarde in mijlen of km?  Londense politie gaat gezichtsscantechnologie gebruiken privacy angsten aanwakkeren
Londense politie gaat gezichtsscantechnologie gebruiken privacy angsten aanwakkeren Duurzaamheid in populistische tijden
Duurzaamheid in populistische tijden Wat zijn enkele interessante feiten over arseen?
Wat zijn enkele interessante feiten over arseen?  Hoe de klimaatverandering het landelijke noordoosten zal beïnvloeden:verwacht drie weken hitte
Hoe de klimaatverandering het landelijke noordoosten zal beïnvloeden:verwacht drie weken hitte  Nieuwe bossen kunnen het overstromingsrisico binnen 15 jaar verminderen
Nieuwe bossen kunnen het overstromingsrisico binnen 15 jaar verminderen Is aardgaskinetische of potentiële energie?
Is aardgaskinetische of potentiële energie?  Hoe gebruik je troposfeer in een volledige zin?
Hoe gebruik je troposfeer in een volledige zin?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

