
Wetenschap
Een gas bestaat uit een mengsel neon en argon De rms -snelheid De atomen zijn 350 Welke atomen?
RMS -snelheid begrijpen
De RMS -snelheid van gasdeeltjes is een maat voor hun gemiddelde kinetische energie. Het is gerelateerd aan de temperatuur van het gas en de molaire massa van de gasdeeltjes door de volgende vergelijking:
* v rms =√ (3RT/M)
waar:
* v rms is de wortelgemiddelde snelheid (in m/s)
* r is de ideale gasconstante (8.314 j/mol · k)
* t is de temperatuur (in Kelvin)
* M is de molaire massa van het gas (in kg/mol)
het probleem
U hebt de RMS -snelheid (350 m/s) verstrekt, maar heeft de temperatuur niet gegeven. Dit maakt het onmogelijk om direct de molmassa van het gasmengsel te bepalen.
Dit is waarom:
* De RMS -snelheid wordt beïnvloed door zowel temperatuur als molaire massa Een hogere temperatuur leidt tot hogere RMS -snelheid en een lagere molaire massa leidt ook tot hogere RMS -snelheid.
* Zonder de temperatuur kunnen we de molaire massa niet isoleren.
Hoe op te lossen met meer informatie
Om de molaire massa (en dus de samenstelling van het gasmengsel) te vinden, zou u ook nodig hebben:
1. De temperatuur: Met de temperatuur kunt u de RMS -snelheidsvergelijking gebruiken om de molaire massa te berekenen.
2. De relatieve overvloed van neon en argon: Je zou de bekende molaire massa's van neon (20,18 g/mol) en argon (39,95 g/mol) kunnen gebruiken om de gemiddelde molaire massa van het mengsel te berekenen op basis van hun verhoudingen.
Laat het me weten als je de temperatuur of de relatieve overvloed van neon en argon hebt, en ik kan je helpen de samenstelling van het gasmengsel te berekenen!
 Waarom kan water niet worden gebruikt in plaats van olie om het halfgeleiderspecimen te dopen?
Waarom kan water niet worden gebruikt in plaats van olie om het halfgeleiderspecimen te dopen?  een nieuwe, natuurlijke wascoating maakt kleding waterafstotend en ademend
een nieuwe, natuurlijke wascoating maakt kleding waterafstotend en ademend Hoe sterk zijn krachten tussen atomen in een covalente binding?
Hoe sterk zijn krachten tussen atomen in een covalente binding?  Wat zijn de twee methoden voor het balanceren van chemische vergelijking?
Wat zijn de twee methoden voor het balanceren van chemische vergelijking?  Hoeveel milliliter 0,45 M HCL neutraliseert 25,0 ml 1,00 M KOH?
Hoeveel milliliter 0,45 M HCL neutraliseert 25,0 ml 1,00 M KOH?
 Orkanen:iets sterker, een beetje langzamer, en een stuk natter in een warmer klimaat
Orkanen:iets sterker, een beetje langzamer, en een stuk natter in een warmer klimaat Wetenschappers creëren een nieuw idee over hoe je een opwarmende planeet kunt hacken:het drogen van de bovenste atmosfeer
Wetenschappers creëren een nieuw idee over hoe je een opwarmende planeet kunt hacken:het drogen van de bovenste atmosfeer  Mariene mist komt onder de aandacht in nieuwe vijfjarige studie
Mariene mist komt onder de aandacht in nieuwe vijfjarige studie Opwarming van 2 C zou miljarden tonnen bodemkoolstof vrijgeven
Opwarming van 2 C zou miljarden tonnen bodemkoolstof vrijgeven Dorian roept talloze bedreigingen op voor zuidelijke staten
Dorian roept talloze bedreigingen op voor zuidelijke staten
Hoofdlijnen
- Wat gebeurt er als we menselijke kwaliteiten toekennen aan bedrijven?
- Wat is de overheersende organel in wortelcellen?
- Wetenschappers identificeren genetische mechanismen die betrokken zijn bij de manier waarop vrouwen eigenschappen erven
- Welk vaccin wordt geproduceerd door slechts een deel van het virale genoom te gebruiken?
- Wat is een nucleïnezuur?
- Onderzoeker ontdekt dat houtkikkers snel evolueerden als reactie op strooizout
- Wat is evolutie die zich voordoet gedurende een korte periode die wordt genoemd?
- Contraststelling van reproductieve fenologische strategieën bij ontdekte gematigde houtsoorten
- Nieuw onderzoek wijst uit dat walvistanden na het midden van de dracht nog steeds aanwezig zijn, wat enigszins verrassend is
- Loden leidingen veilig maken

- Onderzoekers ontwikkelen stof die SARS-CoV-2 door contact kan elimineren

- Overlevingsstrategie:hoe één enzym bacteriën helpt herstellen van blootstelling aan antibiotica

- LED-ing the way:een schone en handige methode om kunststof oppervlakken voor de industrie te oxideren

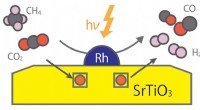
- Milieuvriendelijke katalysator voor het omzetten van methaan in bruikbare gassen met behulp van licht in plaats van warmte
 Materiegolven en kwantumsplinters
Materiegolven en kwantumsplinters Licht voor lithografie kan gedrukte vezels passeren
Licht voor lithografie kan gedrukte vezels passeren Wat is een woord voor een interpretatie van observatie?
Wat is een woord voor een interpretatie van observatie?  Een voorspellingstool voor aardverschuivingen bouwen met Google en AI
Een voorspellingstool voor aardverschuivingen bouwen met Google en AI Piratenaanvallen komen vaker voor in wateren met destructieve visserijpraktijken
Piratenaanvallen komen vaker voor in wateren met destructieve visserijpraktijken Koolmonoxide verandert onder omgevingsdruk in groot defectloos grafeenkristal
Koolmonoxide verandert onder omgevingsdruk in groot defectloos grafeenkristal Wat is een leeflike -structuur die voedsel bevat voor het ontwikkelen van een plant?
Wat is een leeflike -structuur die voedsel bevat voor het ontwikkelen van een plant?  Hoe wordt licht gevormd in termen van energieniveaus?
Hoe wordt licht gevormd in termen van energieniveaus?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

