
Wetenschap
Waarom hebben gassen geen gratis oppervlakken?
* onbepaalde vorm en volume: In tegenstelling tot vloeistoffen en vaste stoffen hebben gassen geen vaste vorm of volume. Ze nemen de vorm en het volume van hun container aan. Dit betekent dat ze de hele ruimte vullen Ze bezetten, zonder een afzonderlijke grens of oppervlak.
* Vrij verkeer van deeltjes: Gasdeeltjes bewegen constant en botsen met elkaar en de wanden van hun container. Deze constante beweging voorkomt dat ze een stabiel oppervlak vormen.
* Zwakke intermoleculaire krachten: De aantrekkelijke krachten tussen gasmoleculen zijn erg zwak. Dit betekent dat er geen significante aantrekkingskracht is tussen moleculen waardoor ze bij elkaar blijven en een oppervlak vormen.
Denk er zo aan: Stel je een kamer vol veerkrachtige ballen voor. Ze stuiteren vrij rond en vullen de hele ruimte. Er is geen duidelijke "oppervlak" van veerkrachtige ballen, alleen een willekeurige verdeling door de kamer. Dit is vergelijkbaar met hoe gasmoleculen zich gedragen.
daarentegen:
* vloeistoffen Heb een gedefinieerd oppervlak, omdat de aantrekkelijke krachten tussen vloeibare moleculen sterk genoeg zijn om ze bij elkaar te houden.
* vaste stoffen Heb een rigide structuur, met moleculen strak gepakt, wat resulteert in een vaste vorm en volume.
Daarom hebben gassen geen vrije oppervlakken vanwege hun gebrek aan een vaste vorm en volume, constante deeltjesbeweging en zwakke intermoleculaire krachten.
 Door de natuur geïnspireerde proteïne kan helpen bij de plasticplaag
Door de natuur geïnspireerde proteïne kan helpen bij de plasticplaag Hoe zou je atomen en aluminium in gasvormige fase veranderen?
Hoe zou je atomen en aluminium in gasvormige fase veranderen?  Video:Hoe scheerschuim werkt
Video:Hoe scheerschuim werkt Betaalbare loodsensor voor thuis, stadswaterleidingen
Betaalbare loodsensor voor thuis, stadswaterleidingen Waarom heeft stikstof een lading van negatieve 3 wanneer deze deelneemt aan chemische reactie?
Waarom heeft stikstof een lading van negatieve 3 wanneer deze deelneemt aan chemische reactie?
 Onverwachte facetten van Antarctica komen naar voren uit de laboratoria
Onverwachte facetten van Antarctica komen naar voren uit de laboratoria Cuba evacueert 180, 000 als tropische storm Elsa nadert
Cuba evacueert 180, 000 als tropische storm Elsa nadert Bos Welke voordelen heeft een brand voor levende wezens?
Bos Welke voordelen heeft een brand voor levende wezens?  Wereld verlengt reeks warmterecords voor de elfde maand op rij
Wereld verlengt reeks warmterecords voor de elfde maand op rij  Professor maakt visualisatietool voor klimaatgegevens die veranderingen in de atmosfeer in realtime kan onthullen
Professor maakt visualisatietool voor klimaatgegevens die veranderingen in de atmosfeer in realtime kan onthullen
Hoofdlijnen
- Wat hebben andere dieren dat haar?
- Zijn de bases van RNA a g c en u?
- Hoe zit het met een object, wordt het soort materie waaruit het bestaat en de manier waarop het is gerangschikt genoemd?
- Wat is het belangrijkste kenmerk dat plantencellen niet hebben?
- Hoe worden de noliverende delen van een ecosysteem genoemd?
- Is het Golgi -lichaam meestal bedekt met ribosomen?
- Wat is een voorbeeld van een organisme dat zich seksueel voortplant en de diversiteit van zijn nakomelingen verklaart?
- De vorm van een combinatie twee eigenschappen die verborgen kunnen worden, wordt eigenschap genoemd?
- Doen probiotica echt iets? | Hoe dingen werken
- Nieuw pad naar vorming van zeldzame aardmineralen heeft gevolgen voor groene energie en slimme technologie

- Katalysatoroppervlakken actiever maken om brandstoffen en chemicaliën koolstofarm te maken
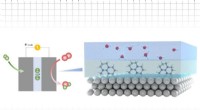
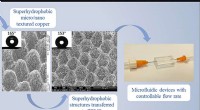
- Nieuw productieproces creëert superkleine kanalen om water af te weren en medische, elektronische apparaten
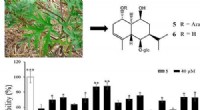
- Ambrosia-verbindingen kunnen zenuwcellen beschermen tegen Alzheimer
- Ontdekken wat durian doet stinken

 Quantumtechnologieën versnellen met materiaalverwerking op atomaire schaal
Quantumtechnologieën versnellen met materiaalverwerking op atomaire schaal Hoe Herschel de geheimen van stervorming ontsloot
Hoe Herschel de geheimen van stervorming ontsloot Tijdkristallen en topologische supergeleiders versmelten
Tijdkristallen en topologische supergeleiders versmelten Welke planeet heeft jaren langer dan zijn dagen?
Welke planeet heeft jaren langer dan zijn dagen?  Onderzoekers ontwerpen polymeer dat resistente bacteriën kan doden
Onderzoekers ontwerpen polymeer dat resistente bacteriën kan doden Hoe wordt warmte van een radiatoroverdracht?
Hoe wordt warmte van een radiatoroverdracht?  Grondstoffen achter helft van wereldwijde emissies:UN
Grondstoffen achter helft van wereldwijde emissies:UN Hoe vind je een soortelijk gewicht van ijzererts?
Hoe vind je een soortelijk gewicht van ijzererts?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

