
Wetenschap
Wat is de structuur van zwavelmonochloride S2CL2?
* Moleculaire geometrie: gebogen (vergelijkbaar met water, h₂o).
* Bindhoeken: Ongeveer 103 ° (iets minder dan de ideale tetraëdrische hoek van 109,5 °).
* Hybridisatie: De zwavelatomen zijn spdat gehybridiseerd .
* binding: Elk zwavelatoom vormt een enkele binding met het andere zwavelatoom en een enkele binding met elk chlooratoom.
Hier is een uitsplitsing van de structuur:
1. Centraal atoom: Er zijn twee zwavelatomen in het midden van het molecuul.
2. rondom atomen: Elk zwavelatoom is verbonden aan het ene chlooratoom en het andere zwavelatoom.
3. eenzame paren: Elk zwavelatoom heeft twee eenzame paren elektronen.
Representatie:
U kunt de structuur op verschillende manieren vertegenwoordigen:
* Lewis -structuur: Dit toont de binding en eenzame paren als stippen.
* Ball-and-Stick Model: Dit toont de atomen als bollen en de bindingen als sticks.
* Model voor ruimtevullen: Dit toont de relatieve afmetingen van de atomen en de algehele vorm van het molecuul.
Opmerking: De gebogen vorm van S₂cl₂ ontstaat door de afstoting tussen de enige paren op de zwavelatomen.
 Hoe elementen te combineren tot samengestelde vormen
Hoe elementen te combineren tot samengestelde vormen  Wat is een groter watermolecuul of koolstofatoom?
Wat is een groter watermolecuul of koolstofatoom?  Wetenschappers vereenvoudigen het proces om polymeren te maken met door licht geactiveerde nanodeeltjes
Wetenschappers vereenvoudigen het proces om polymeren te maken met door licht geactiveerde nanodeeltjes China verbiedt buitenlands afval – maar wat zal er gebeuren met de recycling in de wereld?
China verbiedt buitenlands afval – maar wat zal er gebeuren met de recycling in de wereld?  Wat zijn sommige banen die een chemicus heeft?
Wat zijn sommige banen die een chemicus heeft?
 Industriële microben kunnen vee voeden, varkens en kippen met minder schade aan het milieu
Industriële microben kunnen vee voeden, varkens en kippen met minder schade aan het milieu Hoe ziet de aarde eruit zonder verwering en erosie?
Hoe ziet de aarde eruit zonder verwering en erosie?  Sterke aardbeving treft Solomons; wat schade maar geen tsunami
Sterke aardbeving treft Solomons; wat schade maar geen tsunami De impact van klimaatverandering op het stroomgebied van de Tana in Kenia
De impact van klimaatverandering op het stroomgebied van de Tana in Kenia Wat is de betekenis van wetenschap?
Wat is de betekenis van wetenschap?
Hoofdlijnen
- What is the definiton a nascassist?
- Elk organisme dat zijn eigen voedsel maakt door fotosynthese is?
- Onderzoek suggereert vrouwelijk voordeel in levensverwachting gerelateerd aan fundamentele biologische wortels
- Luipaarden doden minstens 3 kinderen op het Indiase platteland
- Gespecialiseerde cellen in het lichaam
- Hoeveel ATP-moleculen per glucose krijgt een cel bij elk van de drie stadia van cellulaire ademhaling?
- Welk organisme veroorzaakte de Ierse Patato -plaag?
- Is mitochondria een functie of structuur?
- Chinese fossiele eieren tonen achteruitgang van dinosauriërs voordat ze uitstierven
- Afvalkooldioxide gebruiken om metalen van ertsen te scheiden
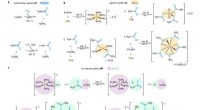
- De deuren openen naar effectieve COVID-19-behandelingen
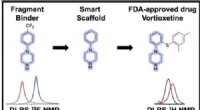
- Een alternatieve route voor het bestuderen van de intrinsieke eigenschappen van vastestofmaterialen

- Hydrogel coating is de eerste om ijsvorming op 3 verschillende manieren te voorkomen

- Van atoom tot natural killer cel:het verhaal van een onverwachte eiwitstructuur
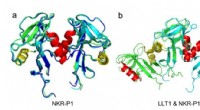
 Hoe wordt het genoemd als licht van richting verandert nadat ze botsen met materie deeltjes?
Hoe wordt het genoemd als licht van richting verandert nadat ze botsen met materie deeltjes?  Van wat voor soort rotsen zijn trottoirs gemaakt?
Van wat voor soort rotsen zijn trottoirs gemaakt?  Kunnen we de koraalrifcatastrofe echt stoppen?
Kunnen we de koraalrifcatastrofe echt stoppen? Hoe behoudt het nemen van een koude douche energie?
Hoe behoudt het nemen van een koude douche energie?  Moleculaire files doorbreken met nanoporeuze materialen met vinnen
Moleculaire files doorbreken met nanoporeuze materialen met vinnen Een isotoop van uranium met behulp van nuclide -notatie?
Een isotoop van uranium met behulp van nuclide -notatie?  Wanneer verzendde de eerste sonde van Mars?
Wanneer verzendde de eerste sonde van Mars?  Slecht nieuws wordt hysterie in menigten, nieuw onderzoek toont aan
Slecht nieuws wordt hysterie in menigten, nieuw onderzoek toont aan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

