
Wetenschap
Als de oplosbaarheid van KHT -kaliumbitartraat toeneemt met de temperatuurstijging, wat kunt u dan zeggen over teken enthalpieverandering KHTWY?
Inzicht in enthalpie -verandering van ontbinding
* Endothermische oplossing: Wanneer warmte wordt geabsorbeerd uit de omgeving tijdens het oplossende proces (enthalpieverandering is positief, ΔH> 0), neemt de oplosbaarheid van de opgeloste stof toe met de temperatuur. Dit komt omdat het systeem probeert meer warmte te absorberen om het endotherme proces te compenseren.
* Exotherme oplossing: Wanneer warmte wordt vrijgegeven in de omgeving tijdens het oplossingsproces (enthalpieverandering is negatief, ΔH <0), neemt de oplosbaarheid van de opgeloste stof af met de temperatuur. Dit komt omdat het systeem al warmte vrijgeeft, dus het verder verhogen van de temperatuur zou het evenwicht verstoren.
het toepassen op KHT
Omdat de oplosbaarheid van KHT toeneemt met de temperatuur, kunnen we concluderen dat de oplossing van KHT endotherm is .
Waarom?
De verhoogde oplosbaarheid bij hogere temperaturen geeft aan dat het systeem warmte absorbeert om het oplossingsproces te bevoordelen. Dit betekent dat de enthalpieverandering (AH) voor de oplossing van KHT positief is.
Samenvattend:
Het feit dat de oplosbaarheid van KHT toeneemt met temperatuur, geeft aan dat de enthalpie -verandering van oplossing (AH) voor KHT positief is. Dit betekent dat het oplossingsproces endotherm is en warmte uit de omgeving absorbeert.
 Wat is het verschil tussen acetyleen en formaldehyde?
Wat is het verschil tussen acetyleen en formaldehyde?  Welke verbinding met zuurstof verklaart waarom er zoveel in je lichaam zit?
Welke verbinding met zuurstof verklaart waarom er zoveel in je lichaam zit?  Is het vermogen om te reageren met andere stoffen chemisch of fysiek?
Is het vermogen om te reageren met andere stoffen chemisch of fysiek?  PNNL-technologie maakt de weg vrij voor van ethanol afgeleide vliegtuigbrandstof
PNNL-technologie maakt de weg vrij voor van ethanol afgeleide vliegtuigbrandstof Wanneer natrium en chloorverbinding, veranderen hun eigenschappen?
Wanneer natrium en chloorverbinding, veranderen hun eigenschappen?
 Wat zou het belang kunnen zijn van culturele ecosysteemdiensten op zee en aan de kust?
Wat zou het belang kunnen zijn van culturele ecosysteemdiensten op zee en aan de kust? Natuurkundigen lossen al lang bestaande puzzel op over hoe motten verre partners vinden
Natuurkundigen lossen al lang bestaande puzzel op over hoe motten verre partners vinden  Rooknevel omhult Sydney terwijl de dreiging van bosbranden toeneemt
Rooknevel omhult Sydney terwijl de dreiging van bosbranden toeneemt Hoe het bestuderen van (robot)duivennavigatie mijn mening over hun intellect veranderde
Hoe het bestuderen van (robot)duivennavigatie mijn mening over hun intellect veranderde  Hoe kan een tent zonne-energie gebruiken?
Hoe kan een tent zonne-energie gebruiken?
Hoofdlijnen
- Beschrijf een orgainssma die alleen als een groep cellen kan bestaan?
- Nieuwe studie heeft tot doel de redenen te begrijpen waarom genitale snijden bij vrouwen aanhoudt (update)
- Wat zijn de functies van mRNA & tRNA?
- Juice:Waarom duurt het zo lang?
- Hoe ontstaan vliegen?
- Wat is de fysiologische activiteit in de lever, milt en dikke darm?
- Wat is de verdediging van de wetenschap?
- Welke vertakkingsstructuren dragen informatie naar het cellichaam van een neuron?
- Hebben bacteriën enzymen voor het uitvoeren van metabole activiteiten?
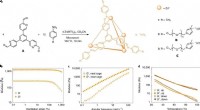
- Poreuze vloeistof bevat grotere moleculen
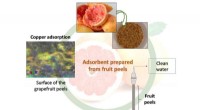
- Afvalwater gereinigd dankzij een nieuw adsorberend materiaal gemaakt van fruitschillen
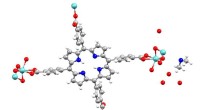
- Wetenschappers persen katalysatoren in gastheermaterialen zoals een schip in een fles

- MOF-gegevensset biedt 10, 000 structuren gratis voor academisch onderzoek
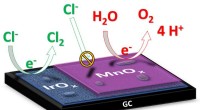
- Een stap dichter bij duurzame energie uit zeewater
 Welke eigenschappen hebben de meeste covalente verbindingen gemeen?
Welke eigenschappen hebben de meeste covalente verbindingen gemeen?  Wat is een geleider van elektriciteit en een isolator -elektriciteit?
Wat is een geleider van elektriciteit en een isolator -elektriciteit?  Heeft Venus ooit zonnige dagen?
Heeft Venus ooit zonnige dagen?  De realisatie van door metingen geïnduceerde kwantumfasen op een quantumcomputer met ingesloten ionen
De realisatie van door metingen geïnduceerde kwantumfasen op een quantumcomputer met ingesloten ionen Hoe ga je laten zien dat je door het uitoefenen van druk materiedeeltjes dicht bij elkaar kunt brengen?
Hoe ga je laten zien dat je door het uitoefenen van druk materiedeeltjes dicht bij elkaar kunt brengen?  Waarom nemen consumenten deel aan 'groene' programma's?
Waarom nemen consumenten deel aan 'groene' programma's?  Hoe zit het met de volgende notaties is de juiste adellijke gasconfiguratie voor SR?
Hoe zit het met de volgende notaties is de juiste adellijke gasconfiguratie voor SR?  Wat vormt een peptidebinding?
Wat vormt een peptidebinding?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

