
Wetenschap
Welk element gedraagt zich chemisch vergelijkbaar met natrium?
Het element dat chemisch vergelijkbaar is met natrium is kalium (k) .
Dit is waarom:
* Ze bevinden zich allebei in dezelfde groep (groep 1, alkali -metalen) van de periodieke tabel. Dit betekent dat ze hetzelfde aantal valentie -elektronen (1) hebben en dus vergelijkbare chemische eigenschappen.
* ze vormen gemakkelijk +1 ionen. Zowel natrium als kalium verliezen één elektron om een stabiele elektronenconfiguratie te bereiken.
* Het zijn zeer reactieve metalen. Ze reageren krachtig met water en lucht en geven waterstofgas vrij.
Terwijl andere elementen in groep 1 ook vergelijkbare eigenschappen hebben als natrium, is kalium het dichtst in de buurt van reactiviteit en gedrag.
 Leg uit hoe we weten hoe de binnenkant van de aarde eruit ziet als we er nog nooit zijn geweest?
Leg uit hoe we weten hoe de binnenkant van de aarde eruit ziet als we er nog nooit zijn geweest?  Hoeveel bomen kan een bij bestoven?
Hoeveel bomen kan een bij bestoven?  3 Voorbeeld van situatie om aan te tonen dat wetenschap om ons heen is en het laboratorium niet beperkt?
3 Voorbeeld van situatie om aan te tonen dat wetenschap om ons heen is en het laboratorium niet beperkt?  Van chaos naar orde:hoe mieren het zoeken naar voedsel optimaliseren
Van chaos naar orde:hoe mieren het zoeken naar voedsel optimaliseren  Aquaria:Jordan laat militaire hardware zinken voor onderwatermuseum
Aquaria:Jordan laat militaire hardware zinken voor onderwatermuseum
Hoofdlijnen
- Wat is een algemeen kenmerk van nucleïnezuren?
- Zijn eicellen bij ouder wordende primaten beschermd tegen mutaties?
- Reproductieproces bij mensen
- Uit onderzoek blijkt hoe de zebravis aan zijn streep komt
- Leg uit hoe hypertoniciteit kan worden gebruikt als een middel om microbiële groei te beheersen?
- Hoe en waarom is het oog voortgekomen door natuurlijke selectie?
- Camera's leggen openhartig bushmeat-zoogdieren vast voor lokale monitoring van dieren in het wild
- Hoe een 'vuurvlieg'-worm te construeren
- Waarom gebruiken wetenschappers modellen van natuurlijke systemen die uw antwoord niet vertellen?
- Industriële verbinding krijgt milieuvriendelijke reactie
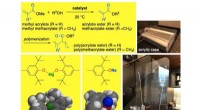
- Proces zet polyethyleen zakken, plastics om in polymere bouwstenen
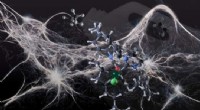
- Synthetisch gelatineachtig materiaal bootst de rek en sterkte van de onderbuik van kreeft na
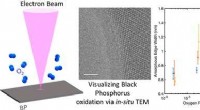
- Ingenieurs bevorderen inzichten over zwarte fosfor als materiaal voor toekomstige flexibele elektronica met ultralaag vermogen
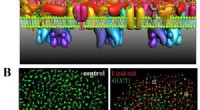
- Beeldvorming met superresolutie onthult het mechanisme van GLUT1-clustering
 Wat is ademhaling en cellulair, hoe zijn ze gerelateerd?
Wat is ademhaling en cellulair, hoe zijn ze gerelateerd?  22 cm gelijk hoeveel inches?
22 cm gelijk hoeveel inches?  Hier is hoe wetenschappers het volgende orkaanseizoen voorspellen
Hier is hoe wetenschappers het volgende orkaanseizoen voorspellen  Bij zonnecellen, het tweaken van de kleinste onderdelen levert een grote sprong in efficiëntie op
Bij zonnecellen, het tweaken van de kleinste onderdelen levert een grote sprong in efficiëntie op Is het hennep of marihuana? Nieuwe scanner geeft direct antwoord
Is het hennep of marihuana? Nieuwe scanner geeft direct antwoord  Nieuwe beeldvormingstechniek laat zien hoe DNA wordt beschermd aan de uiteinden van chromosomen
Nieuwe beeldvormingstechniek laat zien hoe DNA wordt beschermd aan de uiteinden van chromosomen  Welke factor beïnvloedt de hoeveelheid stralende energie op aarde?
Welke factor beïnvloedt de hoeveelheid stralende energie op aarde?  Gewoon een faag? Hoe de roofdieren van bacteriën het darmmicrobioom kunnen vormen
Gewoon een faag? Hoe de roofdieren van bacteriën het darmmicrobioom kunnen vormen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

