
Wetenschap
Wanneer bindingen zich tussen koolstof en waterstof of zuurstof in het algemeen bevinden, wat voor soort binding?
Dit is waarom:
* Covalente bindingen betrokken zijn bij het delen van elektronen tussen atomen. Koolstof, waterstof en zuurstof hebben allemaal een vergelijkbare elektronegativiteit (vermogen om elektronen aan te trekken), zodat ze de neiging hebben om elektronen te delen in plaats van ze volledig over te dragen (wat een ionische binding zou creëren).
Laten we het afbreken:
* Koolstof-hydrogen (C-H) bindingen: Dit zijn niet -polaire covalente bindingen omdat koolstof en waterstof zeer vergelijkbare elektronegativiteiten hebben. De elektronen worden bijna gelijk gedeeld.
* Koolstof-zuurstof (C-O) bindingen: Dit zijn polaire covalente bindingen omdat zuurstof meer elektronegatief is dan koolstof. De elektronen worden gedeeld, maar het zuurstofatoom trekt de gedeelde elektronen sterker aan, waardoor een lichte negatieve lading op de zuurstof en een lichte positieve lading op de koolstof ontstaat.
Samenvattend: De bindingen tussen koolstof, waterstof en zuurstof zijn voornamelijk covalente bindingen, waarbij de C-H-bindingen niet-polair zijn en de C-O-bindingen polair zijn.
 Zestien doden, 500, 000 geëvacueerd omdat het westen van de VS uit de hand loopt (update)
Zestien doden, 500, 000 geëvacueerd omdat het westen van de VS uit de hand loopt (update) Voorbeelden van natuurlijke ecosystemen
Voorbeelden van natuurlijke ecosystemen Hoe een mannelijke rivierkreeft van een vrouw te vertellen
Hoe een mannelijke rivierkreeft van een vrouw te vertellen
Langoesten zijn kleine, kreeftachtige schaaldieren die over de hele wereld in zoet water leven. Langoesten behoren tot de orde Decopoda, die kreeften en krabben omvat. Ongeveer 450 soorten
 Hoe correleert de variatie in lichaamsgrootte met de migratieprestaties onderweg van een trekvogel over lange afstanden?
Hoe correleert de variatie in lichaamsgrootte met de migratieprestaties onderweg van een trekvogel over lange afstanden?  Het effect van aluminium blikjes op de omgeving
Het effect van aluminium blikjes op de omgeving
Hoofdlijnen
- Welk distributiepatroon heeft geen volgorde om te worden verdeeld via een ecosysteem?
- In welk pH -niveau overleeft de meeste organismen?
- Hoe verschillen koolhydraten -eiwitten en lipiden in structuurfunctie?
- Waarom is de pelycosaurus een verband tussen zoogdieren en reptielen?
- Lemur-studie benadrukt de rol van voeding bij het vormgeven van het darmmicrobioom
- Wat bevat het ruwe endoplasmatische materiaal dat het gladde reticulum niet heeft?
- Onderzoekers tonen een nieuwe holistische benadering van genetica en plantenveredeling
- Beschrijf de verschillende kenmerken van het leven?
- Verschil tussen transcriptie en DNA-replicatie
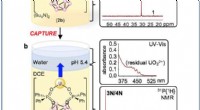
- Team ontwikkelt een elektrochemische methode om uranium te winnen, en mogelijk andere metaalionen, van oplossing
- Een nieuwe manier om met zonlicht schone waterstofbrandstof te maken uit water

- Goud delven met een computer

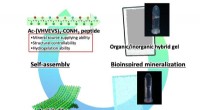
- Bio-geïnspireerde mineralisatie van calciumcarbonaat in peptide hydrogel
- Een nieuwe strategie om koolstofnitride-fotokatalysatoren voor stikstofreductie te stabiliseren

 Waarom is de omgeving belangrijk?
Waarom is de omgeving belangrijk?  Welke gassen zijn de belangrijkste componenten van de zon?
Welke gassen zijn de belangrijkste componenten van de zon?  Diffirinaat toegepaste wetenschap en pure wetenschap?
Diffirinaat toegepaste wetenschap en pure wetenschap?  Wat is de definitie van Gregor Mendel?
Wat is de definitie van Gregor Mendel?  Het volgende idee van SpaceX:vang superzware boosters met de lanceertoren
Het volgende idee van SpaceX:vang superzware boosters met de lanceertoren Warmte kan door wat worden overgedragen?
Warmte kan door wat worden overgedragen?  Wat is de dichtstbijzijnde ster tot aarde?
Wat is de dichtstbijzijnde ster tot aarde?  Hoe de PH van NaOH
Hoe de PH van NaOH
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

