
Wetenschap
Wat is de evenwichtige vergelijking voor de reactie van ammoniakdamp en waterstofsulfidegas om vast ammoniumsulfide te produceren?
2 NH₃ (G) + H₂s (G) → (NH₄) ₂S (S)
Hier is de uitsplitsing:
* 2 NH₃ (G): Dit vertegenwoordigt twee moleculen ammoniakgas (NH₃). De (g) geeft aan dat het zich in de gasvormige toestand bevindt.
* h₂s (g): Dit vertegenwoordigt één molecuul waterstofsulfidegas (H₂S). De (g) geeft aan dat het zich in de gasvormige toestand bevindt.
* (nH₄) ₂s (s): Dit vertegenwoordigt één molecuul van vast ammoniumsulfide ((NH₄) ₂S). De (s) geven aan dat het zich in de vaste toestand bevindt.
Verklaring:
* De reactie omvat twee ammoniakmoleculen (NH₃) die reageren met één waterstofsulfidemolecuul (H₂S).
* Het waterstofsulfidemolecuul levert het sulfide -ion (S²⁻).
* De ammoniakmoleculen bieden de ammoniumionen (NH₄⁺).
* Deze ionen combineren om het solide ammoniumsulfide ((NH₄) ₂s) te vormen.
Deze vergelijking is in evenwicht omdat er zijn:
* 2 stikstofatomen Aan beide zijden van de vergelijking.
* 8 waterstofatomen Aan beide zijden van de vergelijking.
* 1 zwavelatoom Aan beide zijden van de vergelijking.
 De hoeveelheid energie die nodig is om één mol elektronen uit natriumatomen te verwijderen is de?
De hoeveelheid energie die nodig is om één mol elektronen uit natriumatomen te verwijderen is de?  Waar staat de chemische formule NUCO2 voor?
Waar staat de chemische formule NUCO2 voor?  Wat is het kation in zilvernitraat?
Wat is het kation in zilvernitraat?  Wat is de isomeer van azijnzuur?
Wat is de isomeer van azijnzuur?  Onderzoekers ontdekken hoe de enzymomgeving de snelheid en richting van een reactie verandert
Onderzoekers ontdekken hoe de enzymomgeving de snelheid en richting van een reactie verandert
 Wat is ununennium?
Wat is ununennium?  Om de bosbrandcrisis in Australië te begrijpen, moet je moeilijke vragen stellen - en naar de antwoorden luisteren
Om de bosbrandcrisis in Australië te begrijpen, moet je moeilijke vragen stellen - en naar de antwoorden luisteren NASA ziet een nieuwe depressievorm na een andere sisser
NASA ziet een nieuwe depressievorm na een andere sisser Moderne rekenkracht kan toekomstige overstromingsrampen helpen verminderen
Moderne rekenkracht kan toekomstige overstromingsrampen helpen verminderen Pandemische rijreducties zullen de uitstoot van broeikasgassen niet veel verminderen
Pandemische rijreducties zullen de uitstoot van broeikasgassen niet veel verminderen
Hoofdlijnen
- Het beste doel om DNA -replicatie te beschrijven is?
- Kalkhoudende slijk is een voorbeeld van.
- Uit onderzoek blijkt waarom veel IVF-embryo's zich niet ontwikkelen
- Zonder goed beheer raakt de Braziliaanse Cerrado misvormd en minder veerkrachtig tegen de klimaatverandering
- Kun je metabolisme en uitscheiding definiëren?
- Twee nieuwe ontdekkingen werpen licht op het mysterie van hoe cellen met stress omgaan
- Hoe veilig zijn zeevruchten?
- Wat is de primaire functie van DNA?
- Wat gebeurt er na mitose om twee dochtercellen te produceren?
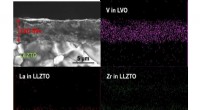
- Kathodefabricage voor oxide solid-state batterijen bij kamertemperatuur
- Energie-efficiënte fotochemie op zonne-energie met luminescente zonneconcentratoren

- Mica geeft een idee van hoe water mineralen transporteert

- Chemici melden biohernieuwbaar, biologisch afbreekbaar plastic alternatief

- Bipolaire volgorde:een eenvoudige techniek om meer controle te hebben over organische dunne films

 Hoe spieren zich ontwikkelen:een dans van cellulaire skeletten
Hoe spieren zich ontwikkelen:een dans van cellulaire skeletten  Is er licht in de ruimte?
Is er licht in de ruimte?  Wat is lof over de wetenschap en welke kritische wetenschap?
Wat is lof over de wetenschap en welke kritische wetenschap?  Genexpressie in Prokaryotes
Genexpressie in Prokaryotes  Experts:enorme archeologische vindplaats onder water in Mexico
Experts:enorme archeologische vindplaats onder water in Mexico Eerste seismisch bewijs voor opgraving van mantels in een ultraslow-verspreidingscentrum
Eerste seismisch bewijs voor opgraving van mantels in een ultraslow-verspreidingscentrum Welk natuurkundig principe verklaart waarom een watersproeier ronddraait?
Welk natuurkundig principe verklaart waarom een watersproeier ronddraait?  Zijn uiteenlopende plaatgrenzen geassocieerd met gevouwen bergen en diepzee -loopgraven?
Zijn uiteenlopende plaatgrenzen geassocieerd met gevouwen bergen en diepzee -loopgraven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

