
Wetenschap
Wat is het massapercentage van H in ammoniumbicarbonaat?
Hier leest u hoe u het massapercentage van H in ammoniumbicarbonaat (NH₄HCO₃) kunt berekenen:
1. Vind de molaire massa van ammoniumbicarbonaat:
* N:14.01 g/mol
* H:1,01 g/mol (x 5) =5,05 g/mol
* C:12.01 g/mol
* O:16.00 g/mol (x 3) =48,00 g/mol
Totale molaire massa =14,01 + 5,05 + 12.01 + 48.00 = 79.07 g/mol
2. Bereken de massa waterstof in één mol ammoniumbicarbonaat:
* Massa van h =5,05 g/mol
3. Bereken het massa -percentage waterstof:
* Massa procent van H =(massa H / molaire massa van NH₄HCO₃) x 100%
* Massa procent van H =(5,05 g/mol/79,07 g/mol) x 100%
* Massa procent van h =6,39%
Daarom is het massa -percentage waterstof in ammoniumbicarbonaat ongeveer 6,39%.
 Stel dat een ander onbekend zuur, sterke zuren, een diagram zijn om de deeltjes opgelost in water weer te geven en dit te beschrijven?
Stel dat een ander onbekend zuur, sterke zuren, een diagram zijn om de deeltjes opgelost in water weer te geven en dit te beschrijven?  Wat is de elektroventie van kalium in sulfaat?
Wat is de elektroventie van kalium in sulfaat?  Wat geeft een chemische eigenschap substantie het vermogen om te doen?
Wat geeft een chemische eigenschap substantie het vermogen om te doen?  Bepaal hoeveel mol BA (OH) 2 nodig zijn om 0,452 mol HC2H3O2 volledig te neutraliseren?
Bepaal hoeveel mol BA (OH) 2 nodig zijn om 0,452 mol HC2H3O2 volledig te neutraliseren?  Wat is de chemische formule van kopernitraat?
Wat is de chemische formule van kopernitraat?
 Potentiële tropische cycloon 10 weken Midden-Atlantische Oceaan
Potentiële tropische cycloon 10 weken Midden-Atlantische Oceaan Studie bevestigt meer media-aandacht voor klimaatverandering gewenst
Studie bevestigt meer media-aandacht voor klimaatverandering gewenst Welke kleuren zijn vleermuizen?
Welke kleuren zijn vleermuizen?  Welk organisme staat misschien aan de top van de voedselketen in een bladverliezend bos?
Welk organisme staat misschien aan de top van de voedselketen in een bladverliezend bos?  Onderschatten we de voordelen van investeren in duurzame energie?
Onderschatten we de voordelen van investeren in duurzame energie?
Hoofdlijnen
- Wat zijn de drie belangrijkste sekten van hersenen?
- Waar komt het woorddichtheid vandaan?
- Wat betekent witte bloedcellen?
- Kan een enkele soort ontleders het dode lichaam volledig uiteenvallen?
- Wat is het eindresultaat van bemesting in termen van chromosomen -getallen?
- Umami-rijke schrootvissen en invasieve soorten kunnen groenten verlevendigen, zegt gastrofysicus
- Wetenschappers onthullen een nieuwe weg naar het verhogen van de borstvoeding voor moeders die borstvoeding geven
- Wat is organische ontwikkeling?
- Uit onderzoek blijkt dat plastic vezels de groei van mosselen met meer dan een derde belemmeren. Dit is waarom dit zorgwekkend is
- Neutronen schilderen atomair portret van prototypisch celsignaleringsenzym
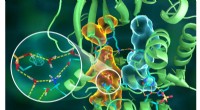
- Synthetisch slijm kan het echte werk nabootsen
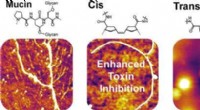
- Autoplastics omzetten in schuim met kokosolie

- Onderzoekers ontwikkelen brandvertragende coating met hernieuwbare materialen

- Glashelder maken:kristalliniteit vermindert de weerstand in volledig solid-state batterijen
 Kun je elektriciteit door lucht verzenden?
Kun je elektriciteit door lucht verzenden?  Waarom heeft de zon de meeste zwaartekracht in jullie zonnestelsel?
Waarom heeft de zon de meeste zwaartekracht in jullie zonnestelsel?  Welke vorm van bacterie is tyfus?
Welke vorm van bacterie is tyfus?  DNA-analyse toont aan dat Griffin Warrior zijn Griekse thuisland regeerde
DNA-analyse toont aan dat Griffin Warrior zijn Griekse thuisland regeerde Aardbeving treft grensgebied Iran-Irak
Aardbeving treft grensgebied Iran-Irak Nieuwe door NASA gefinancierde CubeSat klaar om de temperatuur van de aarde vanuit de ruimte op te nemen
Nieuwe door NASA gefinancierde CubeSat klaar om de temperatuur van de aarde vanuit de ruimte op te nemen Wat zijn enkele items die elektromagneten gebruiken?
Wat zijn enkele items die elektromagneten gebruiken?  GPM Satellite ziet Jebi als een nieuwe tropische bedreiging voor Japan
GPM Satellite ziet Jebi als een nieuwe tropische bedreiging voor Japan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

