
Wetenschap
Betekent een pH -waarde een bepaald aantal waterstof- of hydroxide -ionen?
Dit is waarom:
* pH =-log [H+] waarbij [H+] de concentratie waterstofionen in mol is per liter (M).
* De schaal is logaritmic , wat betekent dat elke gehele getalverandering in pH een tienvoudige verandering in waterstofionconcentratie vertegenwoordigt.
* Een lagere pH duidt op een hogere concentratie waterstofionen , waardoor de oplossing zuurder wordt.
* Een hogere pH duidt op een lagere concentratie waterstofionen , waardoor de oplossing eenvoudiger wordt (alkalisch).
Hoewel pH niet direct het exacte aantal ionen geeft , het kennen van de pH stelt u in staat om de concentratie waterstofionen te berekenen:
* [H+] =10^-ph
Voorbeeld:
* Een oplossing met een pH van 3 heeft een waterstofionconcentratie van 10^-3 m (of 0,001 m).
* Een oplossing met een pH van 10 heeft een waterstofionconcentratie van 10^-10 M.
Belangrijke opmerking:
* De relatie tussen pH en hydroxide -ionen is omgekeerd . Een hogere pH duidt op een lagere concentratie hydroxide -ionen en vice versa.
* Het product van waterstofionconcentratie en hydroxide -ionenconcentratie is constant (KW =10^-14 bij 25 ° C).
Daarom kunt u de pH van een oplossing kennende de relatieve concentratie van waterstofionen en hydroxide -ionen bepalen, maar het biedt niet het exacte aantal aanwezige ionen.
 Team ontwikkelt robuuste moleculaire propeller voor unidirectionele rotaties
Team ontwikkelt robuuste moleculaire propeller voor unidirectionele rotaties Wat is een pure stof die niet kan worden opgesplitst in andere stoffen op chemische of fysieke middelen?
Wat is een pure stof die niet kan worden opgesplitst in andere stoffen op chemische of fysieke middelen?  De zoutoplansflessen die in het laboratorium zijn weggelaten, worden de tijd bedekt met wit poeder een mogelijke samenstelling voor dit waarom ammoniakbacome minder dan HCl?
De zoutoplansflessen die in het laboratorium zijn weggelaten, worden de tijd bedekt met wit poeder een mogelijke samenstelling voor dit waarom ammoniakbacome minder dan HCl?  Onderzoekers ontwikkelen ultrasterke aerogels met materialen die worden gebruikt in kogelwerende vesten
Onderzoekers ontwikkelen ultrasterke aerogels met materialen die worden gebruikt in kogelwerende vesten Waarom wordt melamine gebruikt voor brandwerende uniformen?
Waarom wordt melamine gebruikt voor brandwerende uniformen?
 Gevarieerde voorspellingen voor organische stof in de bodem als klimaatveranderingen
Gevarieerde voorspellingen voor organische stof in de bodem als klimaatveranderingen Vervuiling van producten:CO2-concurrentie gaat laatste ronde in
Vervuiling van producten:CO2-concurrentie gaat laatste ronde in Een biome-project maken vanuit een schoenendoos
Een biome-project maken vanuit een schoenendoos  Noordelijke veengebieden zullen een deel van hun koolstofdioxideopslagcapaciteit verliezen onder een warmer klimaat
Noordelijke veengebieden zullen een deel van hun koolstofdioxideopslagcapaciteit verliezen onder een warmer klimaat China zegt wrak Iraanse olietanker gelokaliseerd
China zegt wrak Iraanse olietanker gelokaliseerd
Hoofdlijnen
- Wat is praseodymium?
- Klein stuk van een ziekteverwekker dat een immuunrespons genereert?
- Is een blaasje een orgel of organel?
- Welk doel dienen chloroplasten in plantencellen?
- Onderzoekers werpen licht op hoe ‘microbiële donkere materie’ ziekten kan veroorzaken
- Variabel gif:waarom zijn sommige slangen dodelijker dan andere?
- Wat is de hoofdmodus van reproductie voor eukaryotische organismen met één geceleerde eukaryotische organismen?
- Wat is een kenmerk van SAC -schimmels?
- Waar vinden sensorische neuronen en motor in?
- Wetenschappers behalen nieuwe resultaten in de studie van anorganische pigmenten met apatietstructuur

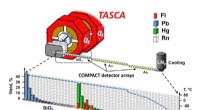
- Onderzoek toont aan dat flerovium het meest vluchtige metaal is in het periodiek systeem
- Onderzoekers gebruiken zijde van zijderupsen om spierweefsel te modelleren

- Marshmallow-achtige siliconengels gebruikt als isolatie in containers voor gecryopreserveerde embryo's

- Nieuw materiaal geïnspireerd op spinnenzijde kan ons plasticprobleem helpen oplossen

 Is het mogelijk voor twee planeten in het zonnestelsel om te botsen?
Is het mogelijk voor twee planeten in het zonnestelsel om te botsen?  Wetenschappers tonen de zwemvaardigheden van Strontium aan
Wetenschappers tonen de zwemvaardigheden van Strontium aan  NASA vindt zware regen in nieuwe tropische cycloon Hilda
NASA vindt zware regen in nieuwe tropische cycloon Hilda Wat is het verschil tussen natuurlijke hulpbronnen en kapitaalbronnen?
Wat is het verschil tussen natuurlijke hulpbronnen en kapitaalbronnen?  Is het waar dat energie nuttig wordt overgedragen in een iPod als thermische energie?
Is het waar dat energie nuttig wordt overgedragen in een iPod als thermische energie?  Game of Thrones-prequel bevestigt dat er geen seksueel geweld op het scherm zal zijn. Dit is waarom dat belangrijk is
Game of Thrones-prequel bevestigt dat er geen seksueel geweld op het scherm zal zijn. Dit is waarom dat belangrijk is Watermeting kan het verbruik met een vijfde verminderen, maar alleen huishoudens met een hoog inkomen verdienen financieel
Watermeting kan het verbruik met een vijfde verminderen, maar alleen huishoudens met een hoog inkomen verdienen financieel Energie van zichtbaar licht kan worden gemeten in georganiseerde pakketten die worden genoemd?
Energie van zichtbaar licht kan worden gemeten in georganiseerde pakketten die worden genoemd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

