
Wetenschap
Wanneer elementair lithiummetaal reageert met elementaire broom, wat is geoxideerd en gereduceerd?
Inzicht in oxidatie en reductie
* oxidatie: Verlies van elektronen. Het oxidatienummer van een element neemt toe.
* reductie: Winst van elektronen. Het oxidatienummer van een element neemt af.
De reactie
De reactie tussen lithium (Li) en broom (Br₂) produceert lithiumbromide (bibliotheek):
2 Li (S) + Br₂ (L) → 2 Libr (s)
Oxidatietoestanden analyseren
* lithium (li):
* Begint als elementair lithium, met een oxidatietoestand van 0.
* In Libr wordt het li⁺, met een oxidatietoestand van +1. Dit betekent dat lithium * een elektron heeft verloren, dus het is geoxideerd .
* bromine (br₂):
* Begint als elementaire broom, met een oxidatietoestand van 0.
* In Libry wordt het br⁻, met een oxidatietoestand van -1. Dit betekent dat Bromine * een elektron heeft gewonnen, dus het is verminderd .
Samenvatting
* lithium wordt geoxideerd. Het verliest een elektron en zijn oxidatietoestand neemt toe van 0 tot +1.
* broom is verminderd. Het krijgt een elektron en zijn oxidatietoestand neemt af van 0 tot -1.
Hoofdlijnen
- Hoe diverse microbiële gemeenschappen stabiel blijven
- Wanneer de vulgreep wordt gebruikt om een cel aangrenzende cellen te kopiëren die wordt genoemd?
- Wat is de volgorde van het neurale pad?
- Is gedenatureerd en gehydrolyseerd eiwit hetzelfde?
- Vasculaire planten kunnen groter worden dan niet -vasculair waar of onwaar?
- Wat maakt jouw stem de jouwe? Onderzoekers ondernemen stappen om de kwaliteit te karakteriseren en te kwantificeren
- Hoe rondwormen beslissen dat de tijd rijp is om te groeien
- Het verschil tussen genomisch DNA en plasmide DNA
- Bijdrage van celstudie door Robert Hooke?
- Bio-geïnspireerde materialen—Grafeen-enabled nikkelcomposieten

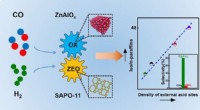
- Directe synthese van isoparaffinerijke benzine uit syngas
- Magnesiumlegering als lichter alternatief voor aluminiumlegering

- Naar een door licht aangedreven moleculaire assembler

- Nieuwe, door licht aangedreven katalysatoren kunnen helpen bij de productie

 Koolstofbelastingen kunnen zowel eerlijk als effectief zijn, studie toont
Koolstofbelastingen kunnen zowel eerlijk als effectief zijn, studie toont Oude Chinese tekst blijkt een anatomische atlas van het menselijk lichaam te zijn
Oude Chinese tekst blijkt een anatomische atlas van het menselijk lichaam te zijn Waarom is het morsen van vloeibare zuurstof bij asfaltbestrating potentieel gevaarlijk?
Waarom is het morsen van vloeibare zuurstof bij asfaltbestrating potentieel gevaarlijk?  De Scutoid:hoe we nieuwe vormen ontdekken
De Scutoid:hoe we nieuwe vormen ontdekken  Chloride -ion zou worden weergegeven door de chemische formule?
Chloride -ion zou worden weergegeven door de chemische formule?  Hoe een animatiestudio 3D-printen gebruikt
Hoe een animatiestudio 3D-printen gebruikt  Vangt cellulaire ademhaling of fotosynthese energie vast?
Vangt cellulaire ademhaling of fotosynthese energie vast?  De ionosfeer groeit tot zijn grootste dikte gedurende welke tijd?
De ionosfeer groeit tot zijn grootste dikte gedurende welke tijd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


