
Wetenschap
Leg uit hoe calcium en fosfaat een verbinding kunnen maken met elektroneutraliteit?
Inzicht in de ladingen
* calcium (CA): Calcium bevindt zich in groep 2 van de periodieke tabel, wat betekent dat het 2 valentie -elektronen heeft. Het heeft de neiging om deze elektronen te verliezen om een stabiel octet te bereiken, waardoor een +2 kation wordt gevormd (ca²⁺).
* fosfaat (po₄³⁻): Fosfaat is een polyatomisch ion bestaande uit één fosforatoom en vier zuurstofatomen. De algehele lading van dit ion is -3 (po₄³⁻).
Het bereiken van elektroneutraliteit
Om een neutrale verbinding te vormen, moeten de positieve en negatieve ladingen in evenwicht zijn. Dit betekent dat we drie calciumionen (ca²⁺) nodig hebben om twee fosfaationen (po₄³⁻) te neutraliseren:
* 3 ca²⁺ (3 x +2 =+6 opladen)
* 2 po₄³⁻ (2 x -3 =-6 lading)
De formule
De resulterende verbinding is ca₃ (po₄) ₂ , dat calciumfosfaat wordt genoemd. De subscriptnummers geven de verhouding van ionen aan die nodig zijn voor elektroneutraliteit.
Verklaring
* 3 ca²⁺ Biedt een totale positieve lading van +6.
* 2 po₄³⁻ Biedt een totale negatieve lading van -6.
* De totale lading is +6 - 6 =0, wat betekent dat de verbinding neutraal is.
Samenvattend
Calcium- en fosfaationen combineren in een specifieke verhouding (3:2) om calciumfosfaat te vormen, Ca₃ (PO₄) ₂, zodat de positieve en negatieve ladingsbalans, resulterend in een elektrisch neutrale verbinding.
 Wat is het verschil tussen koolstofatoom en stikstofatoom?
Wat is het verschil tussen koolstofatoom en stikstofatoom?  Wat initieert chemische reacties door bindingen in de reactanten te verbreken?
Wat initieert chemische reacties door bindingen in de reactanten te verbreken?  Onderzoeken hoe de convergentie van automatisering en AI het onderzoek naar de organische chemie opnieuw vormgeeft
Onderzoeken hoe de convergentie van automatisering en AI het onderzoek naar de organische chemie opnieuw vormgeeft  Stoffen die chemische reacties in levende wezens bevorderen maar niet door de reactie worden beïnvloed, zijn?
Stoffen die chemische reacties in levende wezens bevorderen maar niet door de reactie worden beïnvloed, zijn?  De formule Q is gelijk aan MHF wordt gebruikt om de hoeveelheid warmte te bepalen die wordt geabsorbeerd of afgegeven door een materiaal op het smeltpunt. Waar staan M en HF voor?
De formule Q is gelijk aan MHF wordt gebruikt om de hoeveelheid warmte te bepalen die wordt geabsorbeerd of afgegeven door een materiaal op het smeltpunt. Waar staan M en HF voor?
 Welke dieren in een bladverliezend bos eten de gewone kalk?
Welke dieren in een bladverliezend bos eten de gewone kalk?  Desolate dorpen kampen met hongersnood door droogte in Madagaskar
Desolate dorpen kampen met hongersnood door droogte in Madagaskar Welke woorden beschrijven de landkenmerken die bewijs leverden voor de hypothese?
Welke woorden beschrijven de landkenmerken die bewijs leverden voor de hypothese?  Kunnen drijvende steden mensen helpen zich aan te passen aan de stijgende zeespiegel?
Kunnen drijvende steden mensen helpen zich aan te passen aan de stijgende zeespiegel? Muziekprofessor krijgt patent voor bestrijding van schorskevers die westerse bossen verwoesten
Muziekprofessor krijgt patent voor bestrijding van schorskevers die westerse bossen verwoesten
Hoofdlijnen
- Nieuwe aanpak kan de sleutel zijn tot de behandeling van antibioticaresistente bacteriën
- Wat gorillapoep ons vertelt over evolutie en menselijke gezondheid
- Onderzoeksteam ontwikkelt versneld proces voor genetische verbetering van planteigenschappen
- Vergelijkingen van 4,7 miljoen mtDNA-sequenties laten zien dat GenBank betrouwbaar is voor dier-ID's
- Hoe DNA-profilering werkt
- Hoe kan mitochondriën hun eigen eiwit maken?
- Eindproduct van de Calvin -cyclus?
- Hoe kan mitochondria worden gekoppeld aan fagocytose?
- Waarom is het belangrijk dat levende wezens zich voortplanten?
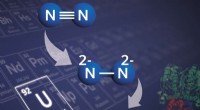
- Een op uranium gebaseerde verbinding verbetert de productie van stikstofproducten
- Een nieuw natuurlijk blauw voor voedselkleuring

- Nieuw voorgestelde strategie biedt slimme flexibele neurale elektrode met hoge efficiëntie
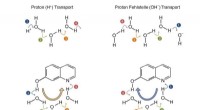
- Vooruit of achteruit? Nieuwe routes voor protonen in water of methanol
- Nieuwe supramoleculaire copolymeren aangedreven door zelfsortering van moleculen

 Zijn slimme horloges het volgende grote ding?
Zijn slimme horloges het volgende grote ding?  Studie zegt dat verzekeringssector gevaarlijk onvoorbereid is op extreem weer
Studie zegt dat verzekeringssector gevaarlijk onvoorbereid is op extreem weer Onderzoekers gebruiken satellietbeelden om het grondwatergebruik in de centrale vallei van Californië in kaart te brengen
Onderzoekers gebruiken satellietbeelden om het grondwatergebruik in de centrale vallei van Californië in kaart te brengen Hebben we een vrije wil en willen we die? Thomas de Stoomlocomotief geeft aanwijzingen
Hebben we een vrije wil en willen we die? Thomas de Stoomlocomotief geeft aanwijzingen Wat is het ABO -systeem?
Wat is het ABO -systeem?  Wat zijn de nadelen van lichtgevende vlammen?
Wat zijn de nadelen van lichtgevende vlammen?  Maanden van zwaartekrachtveranderingen gingen vooraf aan de aardbeving in Tōhoku
Maanden van zwaartekrachtveranderingen gingen vooraf aan de aardbeving in Tōhoku Wat is de concentratie van een oplossing van 450 ml die ijzerchloride van 200 gram bevat?
Wat is de concentratie van een oplossing van 450 ml die ijzerchloride van 200 gram bevat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

