
Wetenschap
Hoeveel gram H20 kan worden geproduceerd door de reactie van 2,40 mol C2 H2 met 7,40 mol O2?
1. Schrijf de gebalanceerde chemische vergelijking:
2 c₂h₂ + 5 o₂ → 4 co₂ + 2 h₂o
2. Bepaal de beperkende reactant:
* Bereken mol h₂o geproduceerd uit 2,40 mol C₂h₂:
- (2.40 mol C₂h₂) * (2 mol H₂o / 2 mol C₂h₂) =2,40 mol H₂o
* Bereken mol h₂o geproduceerd uit 7.40 mol o₂:
- (7,40 mol O₂) * (2 mol H₂o / 5 mol O₂) =2,96 mol H₂o
* De beperkende reactant is c₂h₂ omdat deze de minste hoeveelheid h₂o produceert.
3. Bereken de massa geproduceerde H₂o:
* Gebruik de mol h₂o geproduceerd uit de beperkende reactant (2.40 mol):
- (2.40 mol H₂o) * (18.015 g H₂o / 1 mol H₂o) = 43.24 g H₂o
Daarom kan 43,24 gram h₂o worden geproduceerd door de reactie.
 Als melk zuur wordt, is dat dan een chemische of fysieke verandering?
Als melk zuur wordt, is dat dan een chemische of fysieke verandering?  Welk subatomaire deeltje wordt gevonden in de kern van alle isotopen waterstof?
Welk subatomaire deeltje wordt gevonden in de kern van alle isotopen waterstof?  Nieuwe katalysator voor lagere CO2-uitstoot
Nieuwe katalysator voor lagere CO2-uitstoot Kernwapensimulaties tonen de prestaties tot in moleculair detail
Kernwapensimulaties tonen de prestaties tot in moleculair detail  Welke twee metalen worden gebruikt in een bimetallische strip?
Welke twee metalen worden gebruikt in een bimetallische strip?
 Wat is de beste manier om de uitstoot van broeikasgassen te verminderen?
Wat is de beste manier om de uitstoot van broeikasgassen te verminderen? Wat is de belangrijkste natuurlijke hulpbronnen van Zuidwest -Azië?
Wat is de belangrijkste natuurlijke hulpbronnen van Zuidwest -Azië?  Onze fouten toegeven:wanneer overtreft zelfacceptatie zelfvernietiging?
Onze fouten toegeven:wanneer overtreft zelfacceptatie zelfvernietiging?  Was het een overstroming of niet? Soorten rampen categoriseren in historische gegevens
Was het een overstroming of niet? Soorten rampen categoriseren in historische gegevens Schranklader voor meerdere terreinen Hoe Caterpillar laders en werk
Schranklader voor meerdere terreinen Hoe Caterpillar laders en werk
Hoofdlijnen
- Wat betekent het dat enzymen niet veranderen wanneer ze hun functie uitoefenen?
- Teamrapporten over de relatie tussen de inhoud van diosgenine en brassinosteroïden in Dioscorea zingiberensis
- Wat veroorzaken mutaties in genotype en fenotype?
- Onderzoek laat zien hoe cellen zich herbouwen na mitose
- Wat betekent bacteriën?
- Wat is het type RNA dat informatie van DNA naar het ribosoom draagt, een cel die bekend staat als?
- Hoe protisten de muren van algen kraken
- Ecuador lanceert drijvende eilanden om stinkende monding van Guayaquil te redden
- Wat doen witte bloedcellen met dode cellen?
- Een prachtige moleculaire machine
- Onderzoekers ontwikkelen duurzame methode om vanilline te winnen uit houtverwerkingsafval

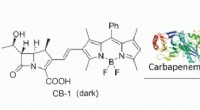
- Een fluorogene sonde kan de activiteit van multiresistente pathogenen in een testsysteem detecteren
- Neutronen zijn bedoeld om de integriteit van ongelijksoortige metaallassen te verbeteren

- De efficiëntie van systemen voor het opvangen en omzetten van koolstof verhogen

 Waarom is niemand op de zon geweest?
Waarom is niemand op de zon geweest?  Substantie wiens kleinste eenheid bestaat uit meer dan één element en kan niet worden gescheiden?
Substantie wiens kleinste eenheid bestaat uit meer dan één element en kan niet worden gescheiden?  Hoe verhoudt het plasmamembraan van de cel zich tot een U-vorm?
Hoe verhoudt het plasmamembraan van de cel zich tot een U-vorm?  Hoe heeft World Hunger het milieu?
Hoe heeft World Hunger het milieu?  Amerikaanse laarzen op de maan in 2024? Het zal niet gemakkelijk zijn
Amerikaanse laarzen op de maan in 2024? Het zal niet gemakkelijk zijn Naar welke verhouding kunt u zich vermenigvuldigen om 26 gallons om te zetten in kwart?
Naar welke verhouding kunt u zich vermenigvuldigen om 26 gallons om te zetten in kwart?  El Niño-rampen:regeringen weten wat er gaat gebeuren, maar zijn niet voorbereid. Dit is wat er moet veranderen
El Niño-rampen:regeringen weten wat er gaat gebeuren, maar zijn niet voorbereid. Dit is wat er moet veranderen  Suiker lost op in water omdat beide uit zijn gemaakt?
Suiker lost op in water omdat beide uit zijn gemaakt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

