
Wetenschap
Schrijf de gebalanceerde vergelijking voor aluminiumhydroxide en natriumnitraat om aluminium te produceren, dank u alsjeblieft?
Aluminiumhydroxide en natriumnitraat reageren niet om aluminium te produceren
* aluminium hydroxide (AL (OH) ₃) is een zwakke basis.
* Natriumnitraat (nano₃) is een zout dat erg oplosbaar is in water en over het algemeen niet reactief.
Deze twee verbindingen zullen, wanneer gemengd, niet reageren om aluminium metaal (AL) te produceren. Dit is waarom:
1. Geen redoxreactie: Een reactie die aluminium metaal zou produceren, zou een reductie van aluminium vereisen van zijn +3 oxidatietoestand in aluminiumhydroxide naar zijn 0 oxidatietoestand in elementair aluminium. Dit soort reactie heeft een sterk reductiemiddel nodig en natriumnitraat is niet sterk genoeg.
2. Geen neerslag: Er is geen onoplosbaar product gevormd dat de reactie vooruit zou brengen. Zowel aluminium nitraat (AL (NO₃) ₃) als natriumhydroxide (NaOH) zijn oplosbaar in water.
wat er eigenlijk gebeurt:
Als u aluminiumhydroxide en natriumnitraat mengt, krijgt u waarschijnlijk een mengsel van deze verbindingen opgelost in water. Er kan een lichte verschuiving in evenwicht zijn vanwege de zwakke basiciteit van aluminiumhydroxide, maar er zal geen significante reactie optreden.
om aluminium metaal te produceren:
Om aluminium metaal te produceren, heb je een proces nodig dat elektrolyse wordt genoemd . Dit omvat het gebruik van elektriciteit om aluminiumionen te dwingen in een gesmolten zoutoplossing om elektronen te krijgen en aluminiumatomen te worden.
Laat het me weten als je andere chemische reacties of het elektrolyseproces wilt verkennen!
 Inzicht in de ferro-elektrische eigenschappen van relaxor kan tot veel vooruitgang leiden
Inzicht in de ferro-elektrische eigenschappen van relaxor kan tot veel vooruitgang leiden Chalk and Vinegar Science Projects
Chalk and Vinegar Science Projects  Waarom heb je 40 gram calcium en 32 zwavel nodig om 72 sulfide te maken?
Waarom heb je 40 gram calcium en 32 zwavel nodig om 72 sulfide te maken?  Is sucrose oplosbaar in natriumhydroxide?
Is sucrose oplosbaar in natriumhydroxide?  Herbruikbare waterbehandelingsdeeltjes elimineren effectief BPA
Herbruikbare waterbehandelingsdeeltjes elimineren effectief BPA
 EU krijgt zware last van vervuiling:eerste normen voor vrachtwagens
EU krijgt zware last van vervuiling:eerste normen voor vrachtwagens Ontdek 200 jaar klimaatverandering in Denemarken, Groenland, en de Faeröer
Ontdek 200 jaar klimaatverandering in Denemarken, Groenland, en de Faeröer Drones tellen de kosten van de 2017 B.C. bosbranden
Drones tellen de kosten van de 2017 B.C. bosbranden Mensen zullen altijd zuurstof hebben om te ademen, maar we kunnen niet hetzelfde zeggen over het leven in de oceaan
Mensen zullen altijd zuurstof hebben om te ademen, maar we kunnen niet hetzelfde zeggen over het leven in de oceaan De bosbrandencrisis trof 75% van de Australiërs:onderzoek
De bosbrandencrisis trof 75% van de Australiërs:onderzoek
Hoofdlijnen
- Hoe kunstmatige intelligentiesystemen de democratie kunnen bedreigen
- Wat zijn de voordelen van eiwitexpressie en zuivering?
- Hoe wordt het lichaamsframe genoemd?
- De beste manieren om bacteriën te kweken op agar
- Welke ontdekking heeft wetenschappers geholpen een beter begrip te krijgen van de menselijke genetica?
- Het bepalen van de manier waarop schimmels tarwe 'smaken' zou de sleutel tot controle kunnen zijn
- Hoe verschilt mitose in de cellen van dieren en planten?
- Vogelgriep heeft melkveehouderijen in Idaho besmet:is de staat voorbereid op een uitbraak?
- In welke fase zit de meeste van de menselijke lichaamscellen?
- Team ontdekt dubbele helixstructuur in synthetisch macromolecuul

- Doorbraak in het benutten van de kracht van biologische katalysatoren

- Nieuwe bacteriële testmethode om de gezondheidszorg te verbeteren, voedselveiligheid en meer
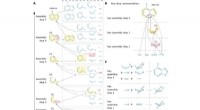
- Assemblagetheorie zou goed nieuws kunnen zijn voor de ontdekking van medicijnen
- Een luchtstabiele en waterdichte lithium-metaalanode

 Langzaam kruipende Dorian een nieuw soort bedreiging
Langzaam kruipende Dorian een nieuw soort bedreiging Wat is de definitie van het systeem in de wetenschap?
Wat is de definitie van het systeem in de wetenschap?  Nieuwste spaak in het wiel drijft brain-mapping vooruitgangen aan
Nieuwste spaak in het wiel drijft brain-mapping vooruitgangen aan Wat zijn de twee regio's van schaduw tijdens een eclips?
Wat zijn de twee regio's van schaduw tijdens een eclips?  Wat gebeurt er als je goud in zoutzuur stopt?
Wat gebeurt er als je goud in zoutzuur stopt?  Onderzoekers ontwikkelen nieuw tumorkrimpend nanodeeltje om kanker te bestrijden herhaling voorkomen
Onderzoekers ontwikkelen nieuw tumorkrimpend nanodeeltje om kanker te bestrijden herhaling voorkomen Wat is de betekenis van Word Life Science?
Wat is de betekenis van Word Life Science?  Welke opkomende feiten over mariene biologie?
Welke opkomende feiten over mariene biologie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

