
Wetenschap
Hoe verschillen Carbon 11 en Boron?
carbon-11
* Atomisch nummer: 6 (wat betekent dat het 6 protonen heeft)
* Atomische massa: 11 (wat betekent dat het 5 neutronen heeft)
* isotoop: Het is een radioactieve isotoop van koolstof, wat betekent dat het onstabiel is en in de loop van de tijd vervalt.
* halfwaardetijd: 20,38 minuten.
* vervalmodus: Positron -emissie.
* Gebruik: Carbon-11 wordt gebruikt in PET (Positron Emission Tomography) scans. Het is opgenomen in moleculen die door het lichaam worden gebruikt, waardoor artsen kunnen zien hoe verschillende organen functioneren.
* Beschikbaarheid: Het wordt geproduceerd met behulp van cyclotrons, die stabiele koolstofatomen bombarderen met protonen.
boron
* Atomisch nummer: 5 (wat betekent dat het 5 protonen heeft)
* Atomische massa: 10.81 (een gemiddelde van verschillende isotopen)
* isotoop: De meest voorkomende boorisotopen zijn stabiel (boron-10 en boron-11).
* halfwaardetijd: Niet van toepassing op de stabiele isotopen.
* vervalmodus: Niet van toepassing op de stabiele isotopen.
* Gebruik: Boron wordt gebruikt in verschillende toepassingen, waaronder:
* Glas en keramiek: Voor zijn vermogen om duurzame, warmtebestendige materialen te vormen.
* halfgeleiders: Als dopingmiddel in silicium voor elektronische apparaten.
* BNCT (borneutron Capture Therapy): Bepaalde isotopen van boor worden gebruikt bij een type kankerbehandeling.
* Beschikbaarheid: Boron wordt op natuurlijke wijze gevonden in de aardkorst en wordt geëxtraheerd uit mineralen.
Samenvattend:
* carbon-11 is een radioactieve isotoop met een korte halfwaardetijd die wordt gebruikt in PET-beeldvorming.
* boron is een stabiel element met verschillende toepassingen, waaronder glas, keramiek, halfgeleiders en behandeling van kanker.
 Lockdown zag een bescheiden daling van de luchtvervuiling in China
Lockdown zag een bescheiden daling van de luchtvervuiling in China Een duurzaam noordpoolgebied moet inheemse groepen omvatten
Een duurzaam noordpoolgebied moet inheemse groepen omvatten Welk ecosysteem heeft vruchtbare grond bedekt met hoog gras?
Welk ecosysteem heeft vruchtbare grond bedekt met hoog gras?  Kelp-DNA registreert vernietigende kracht van oude aardbeving
Kelp-DNA registreert vernietigende kracht van oude aardbeving Het verwijderen van kleine garnalen kan de helderheid van Lake Tahoes helpen klimaatbestendig te maken
Het verwijderen van kleine garnalen kan de helderheid van Lake Tahoes helpen klimaatbestendig te maken
Hoofdlijnen
- Wat zijn fotoblastische cellen?
- Nieuwe CRISPR-tool richt zich op RNA in zoogdiercellen
- Hoe werken de hersenen samen met andere organen in je lichaam?
- Wat is het product van genetische manipulatie?
- Hoe wordt het genoemd als bacteriën zijn gastheer geen pijn doen?
- Welke beschrijven het beste de structuur van DNA?
- Hoe worden organische systemen geactiveerd of gestimuleerd en ontwikkeld door activiteit?
- Wat zijn abiotische dingen en biotische dingen?
- Een gen wiens code niet wordt uitgedrukt tenzij er een soortgelijk allel aanwezig wordt genoemd?
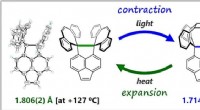
- Covalente koolstof-koolstofbindingen veel flexibeler dan verondersteld
- Giftige PFAS detecteren met een sensor ter grootte van een chip

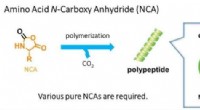
- Het beste van twee werelden:basis-naar-zure flitsschakeling voor organische synthese
- Nieuwe studie onthult dat protonhydratatiestructuren asymmetrisch zijn

- Onderzoekers gebruiken licht om snelle chemische reacties op een nieuwe manier te beheersen

 Hoe ver weg is de dichtstbijzijnde ster tot aarde die de zon niet telt?
Hoe ver weg is de dichtstbijzijnde ster tot aarde die de zon niet telt?  Hoeveel golflengten zijn aanwezig in een kwiklicht?
Hoeveel golflengten zijn aanwezig in een kwiklicht?  Wat is de omtrek van een elektron?
Wat is de omtrek van een elektron?  Welke machine wordt gebruikt om chemische energie te veranderen in bewegingsenergie?
Welke machine wordt gebruikt om chemische energie te veranderen in bewegingsenergie?  Video:informatie kopiëren versus transformeren
Video:informatie kopiëren versus transformeren Windcondities beïnvloeden de watercirculatie en kooldioxideconcentraties in de Zuidelijke Oceaan
Windcondities beïnvloeden de watercirculatie en kooldioxideconcentraties in de Zuidelijke Oceaan Hoe NASA's Curiosity-rover Mars veiliger maakt voor astronauten
Hoe NASA's Curiosity-rover Mars veiliger maakt voor astronauten Lasers -stralen komen in de natuur op waarom of niet?
Lasers -stralen komen in de natuur op waarom of niet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

