
Wetenschap
Hoe is oxidatie in chemie welke staat nano3?
oxidatie in chemie
* Definitie: Oxidatie is een chemisch proces waarbij een stof elektronen verliest. Dit omvat vaak de winst van zuurstofatomen of het verlies van waterstofatomen.
* Sleutelpunten:
* verlies van elektronen: Het kernconcept is het verlies van negatief geladen elektronen.
* toename van de oxidatietoestand: Het element dat oxidatie ondergaat, zal zijn oxidatienummer toenemen.
* vaak met zuurstof: Zuurstof is een zeer elektronegatief element, wat betekent dat het elektronen sterk aantrekt. Het fungeert vaak als een oxidatiemiddel, waardoor andere stoffen elektronen verliezen.
Staat van nano3
* nano3:natriumnitraat Dit is een ionische verbinding, wat betekent dat het wordt gevormd door de elektrostatische aantrekkingskracht tussen positieve en negatief geladen ionen.
* Oxidatie stelt:
* NA (natrium):+1 Natrium bevindt zich in groep 1 van het periodiek systeem, wat betekent dat het meestal één elektron verliest om een +1 kation te vormen.
* n (stikstof):+5 Stikstof bevindt zich in een complexere situatie. In nitraat (NO3-) is de totale lading -1 en heeft zuurstof een -2 -oxidatietoestand (meestal). Om dit in evenwicht te brengen, moet stikstof een +5 oxidatietoestand hebben.
* o (zuurstof):-2 Zuurstof is in groep 16 en vormt meestal een -2 anion.
oxidatie in nano3
* Geen oxidatie of reductie: De oxidatiestaten van de elementen in Nano3 zijn al vastgesteld. De verbinding bevindt zich in een stabiele toestand, zonder verdere overdracht van elektronen die plaatsvinden binnen de verbinding zelf.
Samenvattend
Hoewel oxidatie een fundamenteel concept in de chemie is, gebeurt dit niet binnen de stabiele structuur van NanO3. De verbinding zelf bestaat in een evenwichtige toestand met gedefinieerde oxidatienummers.
 Cyprus:klimaatverandering, achteruitgang op het platteland verhoogt het risico op bosbranden
Cyprus:klimaatverandering, achteruitgang op het platteland verhoogt het risico op bosbranden Wetenschappers ontwikkelen methode om te waarschuwen voor giftige algenbloei voordat ze zich ontwikkelen
Wetenschappers ontwikkelen methode om te waarschuwen voor giftige algenbloei voordat ze zich ontwikkelen Amazones hoogste boom beschermd tegen branden, zeggen wetenschappers
Amazones hoogste boom beschermd tegen branden, zeggen wetenschappers Technologie verbetert rollenspelscenario's voor het beheersen van plotselinge eikendood
Technologie verbetert rollenspelscenario's voor het beheersen van plotselinge eikendood Computermodellen suggereren dat de moderne platentektoniek het gevolg is van klodders die zijn achtergelaten door kosmische botsingen
Computermodellen suggereren dat de moderne platentektoniek het gevolg is van klodders die zijn achtergelaten door kosmische botsingen
Hoofdlijnen
- Zeven nieuwe spinnensoorten uit Brazilië vernoemd naar zeven beroemde fictieve spinnenpersonages
- Is de evolutionaire geschiedenis van een soort of groepsgerelateerde soorten?
- Heeft de kern iets nodig om goed te functioneren?
- Hoe kunnen kinderen van dezelfde ouders er zo verschillend uitzien?
- Wat gebeurt er in plaats van dat het cytoplasma knijpt in de volgende telofaseplantencellen?
- Als onderzoekers niet over de eiwitten beschikken die ze nodig hebben, kunnen ze AI ertoe brengen nieuwe structuren te hallucineren
- Wat is prokryoot?
- Hoe geneest een kikker een gewonde huid zonder littekens?
- Hoe worden bacteriën eigenlijk resistent tegen antibiotica?
- Op zoek naar de zee, en bacteriële gevechten, voor nieuwe antibiotica

- Neutronentomografie:inzicht in het inwendige van tanden, wortel ballen, batterijen, en brandstofcellen

- Nylon als bouwsteen voor transparante elektronische apparaten?

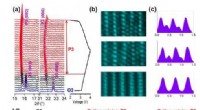
- Kationmenging induceert zeer efficiënte natriumopslag voor gelaagde kathoden
- Onderzoekers ontdekken verborgen ontijzingsrisico's die de gezondheid van de brug beïnvloeden

 Waar komt de energie die in glucose wordt vastgelegd werkelijk vandaan?
Waar komt de energie die in glucose wordt vastgelegd werkelijk vandaan?  DNA-replicatie vergelijken en contrasteren in prokaryoten en eukaryoten
DNA-replicatie vergelijken en contrasteren in prokaryoten en eukaryoten  Een gebogen stuk glas wordt een genoemd?
Een gebogen stuk glas wordt een genoemd?  Wat is tijdhorizon?
Wat is tijdhorizon?  Wat zijn eigenschappen van metaaloïden?
Wat zijn eigenschappen van metaaloïden?  Intel Optane-geheugen H10 met solid-state opslag komt dit jaar uit
Intel Optane-geheugen H10 met solid-state opslag komt dit jaar uit Wanneer wordt elektrische energie geproduceerd?
Wanneer wordt elektrische energie geproduceerd?  De satelliet met röntgenzicht
De satelliet met röntgenzicht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

