
Wetenschap
Hoe schrijft u koolstofdisulfide reageert met zuurstofgas om dioxide- en zwavelgas te produceren?
De gebalanceerde chemische vergelijking voor de reactie van koolstofdisulfide (CS₂) met zuurstofgas (O₂) om koolstofdioxide (CO₂) en zwaveldioxide (SO₂) te produceren is:
CS₂ + 3O₂ → CO₂ + 2SO₂
Hier is een uitsplitsing:
* cs₂: Koolstofdisulfide, de reactant.
* 3o₂: Zuurstofgas, de reactant. Merk op dat de coëfficiënt van 3 nodig is om de zuurstofatomen aan beide zijden in evenwicht te brengen.
* co₂: Koolstofdioxide, het product.
* 2SO₂: Zwaveldioxide, het product. Merk op dat de coëfficiënt van 2 nodig is om de zwavelatomen aan beide zijden in evenwicht te brengen.
Deze vergelijking toont het behoud van massa aan, waarbij hetzelfde aantal atomen van elk element aanwezig zijn aan zowel de reactant als de productkanten.
 Slimme stoffen mogelijk gemaakt door nieuwe metaaldepositietechniek
Slimme stoffen mogelijk gemaakt door nieuwe metaaldepositietechniek Hoe maak je een elektrolyt
Hoe maak je een elektrolyt  Heterogene koperfotokatalyse voor de productie van diverse bioactieve verbindingen
Heterogene koperfotokatalyse voor de productie van diverse bioactieve verbindingen  Lost een koude of hete vloeistof sneller gas op?
Lost een koude of hete vloeistof sneller gas op?  Welke eigenschap hebben de volgende elementen gemeenschappelijk zwavel, jodium en magnesium?
Welke eigenschap hebben de volgende elementen gemeenschappelijk zwavel, jodium en magnesium?
Hoofdlijnen
- Dit is waarom de zwerm zo snel is:de individuen anticiperen op wat de anderen zullen doen
- Sommige planten kunnen de toxische effecten van metalen kortsluiten. Nu proberen wetenschappers hun kracht te benutten
- Welk type plant heeft geen vaatweefsels?
- Wat is het doel van een spore?
- Voorbeelden van organismen waarvan de cellen kernen bevatten?
- Wat zijn de wetenschappelijke variabelen en wat bedoelen ze?
- Is een hoorn des overvloeds homogeen of heterogeen?
- Wat zijn manipulatie van levende organismen om nuttige producten te produceren die worden genoemd?
- Wat zijn enkele voorbeelden van niet-aanpassingen?
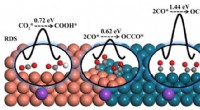
- Afstemming van reactiebarrières voor elektroreductie van kooldioxide tot producten met meerdere koolstofatomen
- Onderzoek naar stikstoffixatie kan licht werpen op biologisch mysterie

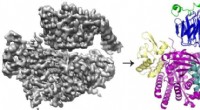
- Studie onthult de ingewikkelde manier waarop twee eiwitten interageren om celbeweging te bevorderen, metastase
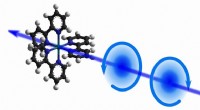
- Chiraliteit in realtime
- Kleurveranderende contactlenzen kunnen de monitoring van oogziektebehandelingen verbeteren

 Wat gebeurt er tijdens vulkaanuitbarstingen?
Wat gebeurt er tijdens vulkaanuitbarstingen?  Wat is een eenvoudige bacterie?
Wat is een eenvoudige bacterie?  Wat is een nadeel van kernenergie?
Wat is een nadeel van kernenergie?  Heeft een ijsblokje energie?
Heeft een ijsblokje energie?  De onderzoeksgroep voert simulaties uit die het klimaat van Zuid-Amerika met ongekende nauwkeurigheid kunnen beschrijven
De onderzoeksgroep voert simulaties uit die het klimaat van Zuid-Amerika met ongekende nauwkeurigheid kunnen beschrijven  Landforms in zoetwatergebieden
Landforms in zoetwatergebieden  Wat is willekeurige moleculaire beweging?
Wat is willekeurige moleculaire beweging?  Wetenschappers ontdekken dat hogere CO₂-niveaus de overleving van virussen in de lucht vergroten en het overdrachtsrisico vergroten
Wetenschappers ontdekken dat hogere CO₂-niveaus de overleving van virussen in de lucht vergroten en het overdrachtsrisico vergroten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

