
Wetenschap
Wat is de evenwichtige halve vergelijking voor broom- en kaliumjodide?
De reactie:
Bromine (Br₂) reageert met kaliumjodide (ki) om jodium (I₂) en kaliumbromide (KBR) te vormen.
De uitgebalanceerde algemene vergelijking:
Br₂ (L) + 2ki (aq) → 2kBr (aq) + i₂ (s)
Half-equations:
1. Oxidatie Half-equation:
* Jodide -ionen (i⁻) worden geoxideerd tot jodium (i₂).
* 2i⁻ (aq) → i₂ (s) + 2e⁻
2. Reductie Half-equation:
* Bromine -moleculen (Br₂) zijn gereduceerd tot bromide -ionen (Br⁻).
* br₂ (l) + 2e⁻ → 2Br⁻ (aq)
Verklaring:
* oxidatie: De jodide -ionen (I⁻) verliezen elektronen en hun oxidatietoestand neemt toe van -1 tot 0.
* reductie: De broommoleculen (Br₂) krijgen elektronen en hun oxidatietoestand neemt af van 0 tot -1.
belangrijke opmerkingen:
* Het aantal verloren elektronen in de oxidatiehalfering moet gelijk zijn aan het aantal dat wordt verkregen in de halfvergelijking van de reductie.
* Dit is de reden waarom we de reductiehalf-equation met 2 vermenigvuldigden.
* Deze halfvergelijkingen kunnen worden gecombineerd om de algehele evenwichtige vergelijking te krijgen.
 Nieuwe cellulaire inzichten in botontwikkeling
Nieuwe cellulaire inzichten in botontwikkeling Koelgordijn gemaakt van een poreus drielaags membraan - alternatief voor elektrisch aangedreven airconditioning
Koelgordijn gemaakt van een poreus drielaags membraan - alternatief voor elektrisch aangedreven airconditioning Wat voor soort symbool wordt gebruikt om aan te tonen dat warmte nodig is bij de ontledingsreactie?
Wat voor soort symbool wordt gebruikt om aan te tonen dat warmte nodig is bij de ontledingsreactie?  Als oplosbaarheid het probleem is, is mechanochemie de oplossing
Als oplosbaarheid het probleem is, is mechanochemie de oplossing Wat vertelt een chemische formule ons over zin?
Wat vertelt een chemische formule ons over zin?
 Hoe ga je de aard bepalen zonder spiegel aan te raken?
Hoe ga je de aard bepalen zonder spiegel aan te raken?  Nieuwe beeldvormingsmethode bekijkt bodemkoolstof op bijna atomaire schaal
Nieuwe beeldvormingsmethode bekijkt bodemkoolstof op bijna atomaire schaal Online tools kunnen mensen helpen bij rampen, maar vertegenwoordigen ze iedereen?
Online tools kunnen mensen helpen bij rampen, maar vertegenwoordigen ze iedereen? Geen plek zoals thuis:nieuwe theorie over hoe zalm en zeeschildpadden hun geboorteplaats vinden
Geen plek zoals thuis:nieuwe theorie over hoe zalm en zeeschildpadden hun geboorteplaats vinden  Geleerden onthullen de veranderende aard van Amerikaanse steden
Geleerden onthullen de veranderende aard van Amerikaanse steden
Hoofdlijnen
- Wat moet een stof bieden om als voedsel te worden beschouwd?
- Wie is de wetenschapper die X Ray Defraction gebruikte om de structuur van DNA te bepalen?
- Producten vervaardigd door Anaerobe Ademhaling
- Is centriolen in dierencel de resaSon waarom plant is verschillend met mitose it?
- Een heroverweging van ziekten in het licht van fasescheiding en faseovergang kan noodzakelijk zijn
- Wetenschappers lossen het mysterie op over hoe het grootste cellulaire motoreiwit beweging aandrijft
- Wat is concurrentie tussen soorten die worden genoemd?
- Wetenschappers leggen uit waarom insecten niet dik worden
- Wat is de vloeistof die de ruimte tussen de kern en het celmembraan vult?
- Een stof in bruinkool kan virussen helpen bestrijden
- Verbinding gevonden in bomen heeft de potentie om resistente bacteriën te doden
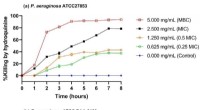
- Onderschatte chemische diversiteit

- Effectief materiaal ontwikkeld om postoperatieve hechting te voorkomen

- Nieuw apparaat kan littekens bij cosmetische chirurgie helpen verminderen
 Kun je vier O -atomen combineren met twee H -atomen?
Kun je vier O -atomen combineren met twee H -atomen?  Wordt de korst gevormd of vernietigd bij een schuifgrens?
Wordt de korst gevormd of vernietigd bij een schuifgrens?  Hoeveel atomen zitten er in 600 gram ijzer?
Hoeveel atomen zitten er in 600 gram ijzer?  Waarom heeft God een komeet gemaakt?
Waarom heeft God een komeet gemaakt?  Waarom twinkelt de zon niet zoals andere sterren?
Waarom twinkelt de zon niet zoals andere sterren?  Een andere naam voor de metamorfe rock genaamd Nice?
Een andere naam voor de metamorfe rock genaamd Nice?  3D-geprinte koralen kunnen bio-energie verbeteren en koraalriffen helpen
3D-geprinte koralen kunnen bio-energie verbeteren en koraalriffen helpen Zelfvouwende origami:Dankzij chemische programmering kunnen Nafion-vellen worden gevouwen en opnieuw gevouwen
Zelfvouwende origami:Dankzij chemische programmering kunnen Nafion-vellen worden gevouwen en opnieuw gevouwen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

