
Wetenschap
Wat worden in een metalen rooster omgeven door pool van elektronen?
Dit is waarom:
* Metallic binding: Metalen vormen een uniek type binding genaamd metallic binding. Bij dit type binding zijn de valentie -elektronen van de metaalatomen niet stevig gebonden aan een specifiek atoom. In plaats daarvan worden ze gedelokaliseerd, wat betekent dat ze vrij kunnen bewegen door het hele rooster.
* Elektronenzee: Deze zee van gedelokaliseerde elektronen werkt als een lijm en houdt de positief geladen ionen bij elkaar in een normale, herhaalde structuur die een rooster wordt genoemd.
* geleidbaarheid: Dit vrije verkeer van elektronen geeft metalen hun karakteristieke eigenschappen, zoals uitstekende elektrische en thermische geleidbaarheid.
Denk er zo aan:stel je de positieve ionen voor als vaste knikkers, en de gedelokaliseerde elektronen als een vloeistof die hen omringt, waardoor ze vrij kunnen bewegen en met elkaar kunnen communiceren.
 Anisotrope plasmonen in quasi-metalen 2-D materialen
Anisotrope plasmonen in quasi-metalen 2-D materialen Hoogbelastende atomair gedispergeerde Ir/MoC-katalysator voor hydrogeneringsreactie
Hoogbelastende atomair gedispergeerde Ir/MoC-katalysator voor hydrogeneringsreactie Waarom zijn vaste stoffen meer oplosbaar in hete vloeistoffen dan koud?
Waarom zijn vaste stoffen meer oplosbaar in hete vloeistoffen dan koud?  Kijkend naar de zijkanten van moleculen:laterale krachtmicroscopie onthult voorheen onzichtbare waterstofatomen
Kijkend naar de zijkanten van moleculen:laterale krachtmicroscopie onthult voorheen onzichtbare waterstofatomen  Welk element vormt een ion met dezelfde lading als ammoniumion?
Welk element vormt een ion met dezelfde lading als ammoniumion?
 Wat waren de eerste organismen die op een rots leven?
Wat waren de eerste organismen die op een rots leven?  Wereldwaterdag 2020:ontziltingstechnologieën zorgen voor veilig en duurzaam drinkwater
Wereldwaterdag 2020:ontziltingstechnologieën zorgen voor veilig en duurzaam drinkwater Regel voor betaalbare schone energie kan leiden tot meer luchtvervuiling en koolstofemissies, studie zegt:
Regel voor betaalbare schone energie kan leiden tot meer luchtvervuiling en koolstofemissies, studie zegt: Ha Long heli:Vietnam lanceert helikopterritten in beroemde baai
Ha Long heli:Vietnam lanceert helikopterritten in beroemde baai Hoe kan materie worden beschreven?
Hoe kan materie worden beschreven?
Hoofdlijnen
- Wat zijn de blaasjes die functioneren in het metabolisme van vetzuren in een cel?
- Osmosis Feiten voor kinderen
- Produceren het licht dat organen produceren van lantaarnvissen gedragsaanpassingen of structurele aanpassingen?
- Wat betekent het als de wetenschap van het plaatsen van tings met vergelijkbare eigenschappen in groepen?
- Waarom is intelligentie bewijs van evolutie?
- Zuurdesem onder de microscoop onthult microben die generaties lang zijn gekweekt
- Wat zijn variaties in specifieke nucleotiden die gekoppeld zijn aan menselijke ziekten?
- Wat is de vloeistof die vrouwelijke sprinkhaan afgeeft tijdens het leggen van eieren?
- Wat voor soort bladvenatie heeft Coriander?
- Bipolaire volgorde:een eenvoudige techniek om meer controle te hebben over organische dunne films

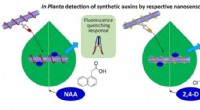
- Onderzoekers ontwerpen sensoren om plantenhormonen snel te detecteren
- Onderzoekers laten protonpomp van ademhalingsketen werken in kunstmatig polymeermembraan

- Een dag om de favoriete eenheid van scheikunde te vieren:de mol. Maar wat is een mol?

- Metaalzepen kritisch in snelheid van bederf van olieverfschilderijen

 De geur van koraal als indicator voor de gezondheid van het rif
De geur van koraal als indicator voor de gezondheid van het rif Hoeveel moleculen zitten er in een korrel zout?
Hoeveel moleculen zitten er in een korrel zout?  Het samenspel tussen wetenschappelijke vooruitgang en geweld in moderne oorlogen
Het samenspel tussen wetenschappelijke vooruitgang en geweld in moderne oorlogen Informatie verkregen uit wetenschappelijk onderzoek wordt genoemd?
Informatie verkregen uit wetenschappelijk onderzoek wordt genoemd?  Wat zijn de sociale kosten van geothermische energie?
Wat zijn de sociale kosten van geothermische energie?  Hebben bacteriecellen een celwand en membraan?
Hebben bacteriecellen een celwand en membraan?  Voordelig beeldvormingssysteem klaar om automatisch muggen te volgen
Voordelig beeldvormingssysteem klaar om automatisch muggen te volgen Nieuwe strategie om katalysatoren met één atoom te fabriceren via elektrochemische depositie
Nieuwe strategie om katalysatoren met één atoom te fabriceren via elektrochemische depositie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

