
Wetenschap
Waarom heb je twee natriumionen nodig voor elk sulfide -ion in sulfide?
* Natrium (NA) bevindt zich in groep 1 van de periodieke tabel: Dit betekent dat natriumatomen de neiging hebben om één elektron te verliezen om positief geladen ionen te worden (Na⁺).
* Zwavel (s) bevindt zich in groep 16 van de periodieke tabel: Dit betekent dat zwavelatomen de neiging hebben om twee elektronen te krijgen om negatief geladen ionen te worden (s²⁻).
Om een neutrale verbinding te vormen, moeten de positieve en negatieve ladingen in evenwicht zijn:
* Eén sulfide -ion (S²⁻) heeft een lading van -2.
* Twee natriumionen (2na⁺) hebben een lading van +2.
Daarom zijn twee natriumionen nodig om de lading van één sulfide -ion te neutraliseren.
Dit zorgt ervoor dat de algehele lading van de verbinding nul is, waardoor deze stabiel is.
 Hoe de klimaatoorlogen te winnen - praat over lokale vervuiling, niet over het broeikaseffect
Hoe de klimaatoorlogen te winnen - praat over lokale vervuiling, niet over het broeikaseffect De zee met de lucht verbinden in het hoge Noordpoolgebied
De zee met de lucht verbinden in het hoge Noordpoolgebied Experiment evalueert het effect van menselijke beslissingen op klimaatreconstructies
Experiment evalueert het effect van menselijke beslissingen op klimaatreconstructies Onderzoekers identificeren verband tussen vaker, intense hitte-evenementen en sterfgevallen in Las Vegas
Onderzoekers identificeren verband tussen vaker, intense hitte-evenementen en sterfgevallen in Las Vegas Afbeelding:Proba-V geeft de fakkel door
Afbeelding:Proba-V geeft de fakkel door
Hoofdlijnen
- Studie van classificatie en naamgeving van planten dieren?
- Hoe verschilt eiwitsynthese in prokaryoten en eukaryote?
- Welke celvorm wordt beat aangepast voor de snelle beweging van stoffen van de ene naar de andere?
- Wat is de rol van celdeling bij het helpen van het lichaam om gezond te blijven?
- Wanneer één referentiegenoom niet genoeg is
- Wat het doel van mitochondria in een cel?
- De mitochondrion is de plaats in cel waar wat er gebeurt?
- Populaties van insecten en bacteriën kunnen snel evolueren omdat ze meestal een korte hebben?
- Conjugatie geeft een eigenschap door van de ene bacterie naar de andere via een kleine DNA-streng die plasmide wordt genoemd. Waar of niet waar?
- Hoe twee isomeren van [IrC₄H₂]⁺ onafhankelijk reageren met methaan of water
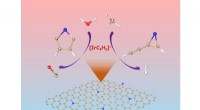
- Nieuwe dynamische sondes voor ionen die interageren met biomoleculen
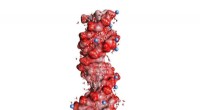
- Elektrochemische cel haalt lithium uit zeewater

- Chemici synthetiseren elektroden voor accu's uit koffiedik
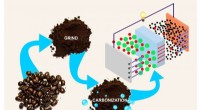
- Nieuw eenvoudig apparaat verbetert de analyse van de reactiekinetiek aanzienlijk
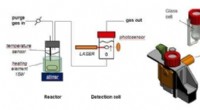
 Welke wetenschapper zei dat het licht een golf is?
Welke wetenschapper zei dat het licht een golf is?  Een land dat u met de breedtegraadmeting van 50 graden North ligt in de?
Een land dat u met de breedtegraadmeting van 50 graden North ligt in de?  Oorlog tegen haaien:hoe malafide vissersvloten het grootste roofdier van de oceaan plunderen
Oorlog tegen haaien:hoe malafide vissersvloten het grootste roofdier van de oceaan plunderen  Wat vormen ingeklapte sterren vormt?
Wat vormen ingeklapte sterren vormt?  Schildpadvriendelijk plastic? Een slimme oplossing voor vervuiling, stroperij en armoede
Schildpadvriendelijk plastic? Een slimme oplossing voor vervuiling, stroperij en armoede  Verrassende aard van solitaire kwantumgolven onthuld
Verrassende aard van solitaire kwantumgolven onthuld Rusland onthult klimaatadaptatieplan
Rusland onthult klimaatadaptatieplan Hoe beïnvloeden uw lengtegraad en breedtegraad het klimaat?
Hoe beïnvloeden uw lengtegraad en breedtegraad het klimaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

