
Wetenschap
Waarom zuurstof verminderd in de reactie van waterstof om water te maken?
* oxidatie: Omvat het verlies van elektronen of een toename in oxidatietoestand.
* reductie: Omvat de winst van elektronen of een afnemen in oxidatietoestand.
Laten we eens kijken naar de reactie:
2h₂ + o₂ → 2h₂o
* waterstof (h₂): Begint met een oxidatietoestand van 0 en eindigt met een oxidatietoestand van +1 in water (H₂o). Dit betekent waterstof wordt geoxideerd .
* zuurstof (o₂): Begint met een oxidatietoestand van 0 en eindigt met een oxidatietoestand van -2 in water (H₂o). Dit betekent dat zuurstof wordt verminderd .
Samenvattend:
* Zuurstof wint elektronen (vermindert) door bindingen met waterstof te vormen.
* Waterstof verliest elektronen (oxideert) door bindingen met zuurstof te vormen.
Dit is een klassiek voorbeeld van een redox -reactie waar het ene element wordt geoxideerd en het andere wordt verminderd.
 Een reactie waarbij een vast product ontstaat, is een voorbeeld van een?
Een reactie waarbij een vast product ontstaat, is een voorbeeld van een?  Wat zijn de reactanten en producten in een verbrandingsreactie?
Wat zijn de reactanten en producten in een verbrandingsreactie?  Nauwe ruimtes tip aanwezigheid van petrochemicaliën
Nauwe ruimtes tip aanwezigheid van petrochemicaliën Wat vind je het minst van in natuur elementen verbindingen of mengsels?
Wat vind je het minst van in natuur elementen verbindingen of mengsels?  Een toekomst van behulpzame engineered living machines?
Een toekomst van behulpzame engineered living machines?
Hoofdlijnen
- Wat voor soort ziekte is tyfus?
- Wat gebeurt er tijdens meiose anafase 1?
- Vergelijkingen van 4,7 miljoen mtDNA-sequenties laten zien dat GenBank betrouwbaar is voor dier-ID's
- Hoe vrije radicalen uw lichaam beïnvloeden
- RNA bevat wat tussen het RNA?
- Wat is dode cel?
- Wat is de wetenschappelijke methode en waarom bestudeer je deze?
- Wat is p-generatie?
- Soorten genetische kruisen
- Wetenschappers breiden PET-beeldvormingsopties uit door eenvoudigere chemie
- Een eenvoudig, goedkoop materiaal voor het afvangen van koolstof, misschien uit uitlaatpijpen

- Octapeptin:Vergeten antibioticum biedt hoop tegen de ergste superbacteriën
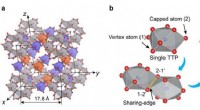
- Doorbraak naar het oplossen van het structurele mysterie van glas
- Innovatiepioniers scoren wereldprimeur voor duurzaam bouwen met grafeenbeton

 Een kracht die elke massa naar een andere massa trekt?
Een kracht die elke massa naar een andere massa trekt?  Wat gebeurt er met een deeltje in vloeistof wanneer verwarmd?
Wat gebeurt er met een deeltje in vloeistof wanneer verwarmd?  Hoe klimaat en waterbeheer de seizoensinvloeden van de stroom beïnvloeden
Hoe klimaat en waterbeheer de seizoensinvloeden van de stroom beïnvloeden  Nieuwe chemische methode kan een revolutie teweegbrengen in grafeen
Nieuwe chemische methode kan een revolutie teweegbrengen in grafeen Zuurtolerant groen fluorescerend eiwit voor bio-imaging
Zuurtolerant groen fluorescerend eiwit voor bio-imaging Wie vloog de Apollo 11 naar de maan?
Wie vloog de Apollo 11 naar de maan?  Bij de grootste uitsterving van de aarde, het afsterven van het land begon lang voordat de oceaan omstroomde
Bij de grootste uitsterving van de aarde, het afsterven van het land begon lang voordat de oceaan omstroomde Hoe ontstaan kristallen door verdamping?
Hoe ontstaan kristallen door verdamping?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

