
Wetenschap
Een waterige oplossing van natriumchloride kan het best geclassificeerd zijn als een?
* elektrolyten zijn stoffen die elektriciteit leiden wanneer opgelost in water. Dit komt omdat ze dissociëren in ionen, die geladen deeltjes zijn die een elektrische stroom kunnen dragen.
* natriumchloride (NaCl) Lost in water op om natriumionen (Na+) en chloride-ionen te vormen (Cl-). Deze ionen zijn vrij om in de oplossing te bewegen, waardoor de oplossing elektriciteit kan leiden.
Laten we het vergelijken met andere opties:
* niet -elektrolyt: Een stof die geen elektriciteit leidt wanneer opgelost in water. Voorbeelden zijn suiker en alcohol.
* zuur: Een stof die waterstofionen (H+) produceert wanneer opgelost in water.
* basis: Een stof die hydroxide-ionen (OH-) produceert wanneer opgelost in water.
Hoewel natriumchloride een aantal basiseigenschappen heeft vanwege de hydroxide -ionen die het vormt in oplossing, wordt het voornamelijk geclassificeerd als een elektrolyt vanwege het vermogen om elektriciteit te leiden.
 Kunstmatig fluorescerend membraanlipide toont actieve rol in levende cellen
Kunstmatig fluorescerend membraanlipide toont actieve rol in levende cellen Wat kan als media fungeren voor een golf A. vaste stoffen B. vloeistoffen C. gassen D. al het bovenstaande?
Wat kan als media fungeren voor een golf A. vaste stoffen B. vloeistoffen C. gassen D. al het bovenstaande?  Moleculen die geen tegengesteld geladen doelen hebben, zijn welke moleculen?
Moleculen die geen tegengesteld geladen doelen hebben, zijn welke moleculen?  Wat is Calgon-proces. Het is het proces om de hardheid van water te verwijderen?
Wat is Calgon-proces. Het is het proces om de hardheid van water te verwijderen?  Sleutelenzymen voor het synthetiseren van natuurlijke producten
Sleutelenzymen voor het synthetiseren van natuurlijke producten
Hoofdlijnen
- Verschil tussen differentiatie en morfogenese
- Meiosis helpt bij evolutie omdat het wat doet?
- Team onthult regels voor het maken van ribben
- Produceert sponsachtig bot rode bloedcellen?
- Welke rol speelde Xray -foto van DNA in de ontdekkingsstructuur?
- Welke van de bases gevonden in RNA?
- Wat is een tweede neef? Het ontrafelen van de stamboom
- Wat wordt er gebruikt om DNA op een specifieke locatie voor splitsing te knippen?
- Wat is het verschil tussen draagvermogen en biotisch potentieel?
- Sensor kan bedorven melk detecteren voor opening

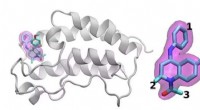
- Een mitochondria-gerichte fluorescerende sonde voor cisplatine
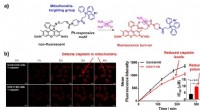
- Onderzoeksgroep gebruikt supercomputing om zich te richten op de meest veelbelovende kandidaat-geneesmiddelen uit een enorm aantal mogelijkheden
- Medewerkers van de röntgenfaciliteit van Berkeley Labs mobiliseren zich om COVID-19-gerelateerd onderzoek te ondersteunen

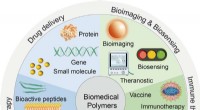
- Biomedische polymeren:synthese, eigenschappen en toepassingen
 Berekening van de vierkante voet op een cube
Berekening van de vierkante voet op een cube Hoeveel mol water is er nodig om te reageren met 2,2 li2o?
Hoeveel mol water is er nodig om te reageren met 2,2 li2o?  Hoe worden vloeistoffen deeltjes verpakt?
Hoe worden vloeistoffen deeltjes verpakt?  Wat is de enthalpie van oplossing ammoniumchloride?
Wat is de enthalpie van oplossing ammoniumchloride?  33 graden Celsius is gelijk aan hoeveel graden Fahrenheit?
33 graden Celsius is gelijk aan hoeveel graden Fahrenheit?  Hoe genereert Frankrijk zijn elektriciteit?
Hoe genereert Frankrijk zijn elektriciteit?  Onderzoekers ontdekken hoe cellen de fysieke toestand van embryonale weefsels controleren
Onderzoekers ontdekken hoe cellen de fysieke toestand van embryonale weefsels controleren  Antropoceen versus Meghalayan - waarom geologen strijden over de vraag of mensen een natuurkracht zijn?
Antropoceen versus Meghalayan - waarom geologen strijden over de vraag of mensen een natuurkracht zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

