
Wetenschap
Hoe is selenium vergelijkbaar met zwavel?
overeenkomsten:
* Elektronische configuratie: Zowel selenium als zwavel hebben zes valentie -elektronen, waardoor ze zeer reactief zijn en vatbaar zijn voor het vormen van anionen met een -2 -lading (bijv. S
2 -
, Se
2-
).
* niet -metalen: Beide zijn niet -metalen, wat betekent dat ze geen metalen eigenschappen missen, zoals geleidbaarheid en kneedbaarheid.
* Vergelijkbare binding: Ze vormen covalente bindingen met andere niet -metalen en ionische bindingen met metalen.
* allotropen: Beide elementen bestaan in verschillende allotrope vormen, wat betekent dat ze verschillende structurele regelingen in hun vaste toestand kunnen hebben. Zwavel bestaat bijvoorbeeld als rhombische en monokliene zwavel, terwijl selenium amorfe en kristallijne vormen heeft.
* Oxidatie stelt: Beide elementen vertonen een breed scala aan oxidatietoestanden, van -2 tot +6, waardoor ze kunnen deelnemen aan diverse chemische reacties.
Er zijn echter ook enkele belangrijke verschillen:
* Atomaire maat: Selenium is groter dan zwavel vanwege de aanwezigheid van een extra elektronenschaal. Dit grootteverschil kan hun reactiviteit en binding beïnvloeden.
* elektronegativiteit: Selenium is minder elektronegatief dan zwavel, wat betekent dat het minder snel elektronen in een binding aanneemt.
* Reactiviteit: Zwavel is over het algemeen reactiever dan selenium.
* Biologische rollen: Selenium is een essentiële micronutriënt voor veel organismen, terwijl zwavel een belangrijk onderdeel is van eiwitten en andere biomoleculen.
Samenvattend:
Selenium en zwavel zijn nauw verwante elementen vanwege hun vergelijkbare elektronische configuratie en positie op het periodiek systeem. Hun atoomgrootte, elektronegativiteit en reactiviteit verschillen echter, wat resulteert in verschillende chemische en biologische eigenschappen.
 Onderzoekers werken samen met kleine bedrijven in NM om nieuwe beademingsmaterialen te testen
Onderzoekers werken samen met kleine bedrijven in NM om nieuwe beademingsmaterialen te testen Wat is het product als Na2Cr2O7 reageert met NaOH?
Wat is het product als Na2Cr2O7 reageert met NaOH?  Een symboolvergelijking voor de thermische ontleding van kopersulfaat?
Een symboolvergelijking voor de thermische ontleding van kopersulfaat?  Wat is de beweging van chemicaliën op wereldwijde schaal van abitotische factoren door biotische omgeving?
Wat is de beweging van chemicaliën op wereldwijde schaal van abitotische factoren door biotische omgeving?  Teams-foto van crack in the act kan technische storingen voorkomen
Teams-foto van crack in the act kan technische storingen voorkomen
 Misleidende mulch:onderzoekers vinden dat de inhoud van mulchzakken niet overeenkomt met de beweringen
Misleidende mulch:onderzoekers vinden dat de inhoud van mulchzakken niet overeenkomt met de beweringen Opkoopkosten voor overstromingen stijgen naarmate de stormen heviger worden, zeeën golfen
Opkoopkosten voor overstromingen stijgen naarmate de stormen heviger worden, zeeën golfen Is een miereneter een herbivoor carnivore of omnivoor?
Is een miereneter een herbivoor carnivore of omnivoor?  Nieuwe studie van aardkorst toont wereldwijde groeispurt van drie miljard jaar geleden
Nieuwe studie van aardkorst toont wereldwijde groeispurt van drie miljard jaar geleden Vulkaan barst uit in Indonesië, alarmniveau verhoogd naar hoogste niveau
Vulkaan barst uit in Indonesië, alarmniveau verhoogd naar hoogste niveau
Hoofdlijnen
- Welke soorten organische moleculen vormen een celmembraan?
- Welke eenheid zou u gebruiken om DNA te meten?
- Een specifiek eiwit dat bepaalde moleculen herkent die ze over het membraan brengen?
- Is het een jongen of is het een meisje? Nieuwe methode om het geslacht van babyzeeschildpadden te identificeren
- Waar hoop je dat het klonen voor volwassenen kan worden gebruikt?
- Welke regio in de hersenen regelt het grootste deel van het onbewuste lichaamsgebied?
- Welke rol spelen anti-oxidanten specifiek in het menselijk lichaam en op de hersenen?
- Leven met een moordenaar:hoe een onwaarschijnlijke associatie tussen bidsprinkhaangarnalen en mosselen het biologische principe schendt
- Onderzoek naar maïsgenetica onthult het mechanisme achter het stil worden van eigenschappen
- Enzymcocktail ontwikkeld in Brazilië stimuleert de productie van ethanol van de tweede generatie

- Een nieuw peptide om multiresistente bacteriën snel te doden

- Vermindering van het corrosieve effect van gesmolten zouten

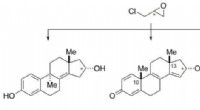
- Onderzoekers ontwikkelen baanbrekend proces om kankerverwekkende medicijnen te maken
- Platinavrije katalysatoren kunnen goedkopere waterstofbrandstofcellen maken

 Hoe wordt de overdracht van lichte energie genoemd?
Hoe wordt de overdracht van lichte energie genoemd?  Wat is volumetrisch opladen?
Wat is volumetrisch opladen?  Wat zijn 3 voorbeelden van elastische kracht?
Wat zijn 3 voorbeelden van elastische kracht?  Wanneer ziektekiemen het lichaam binnengaan, wat zijn antilichamen geproduceerd door?
Wanneer ziektekiemen het lichaam binnengaan, wat zijn antilichamen geproduceerd door?  Ultradunne camera maakt beelden zonder lenzen
Ultradunne camera maakt beelden zonder lenzen Doorbraak bereikt in de verklaring waarom tektonische platen bewegen zoals ze doen
Doorbraak bereikt in de verklaring waarom tektonische platen bewegen zoals ze doen  Onderzoekers ontwikkelen schaal voor diversiteitsintelligentie voor organisaties
Onderzoekers ontwikkelen schaal voor diversiteitsintelligentie voor organisaties Nieuw materiaal opent de mogelijkheid om waterverontreinigende stoffen om te zetten in waterstofgas
Nieuw materiaal opent de mogelijkheid om waterverontreinigende stoffen om te zetten in waterstofgas
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

