
Wetenschap
Wat is de evenwichtige vergelijking van kalium reageert met chloor om chloride te vormen?
Onevenwichtige vergelijking:
K + CL₂ → KCL
Balanced vergelijking:
2K + CL₂ → 2KCL
Verklaring:
* reactanten: Kalium (K) is een metaal en chloor (CL₂) is een diatomee -gas.
* Product: Kaliumchloride (KCL) is een ionische verbinding.
* balanceren:
* Er zijn twee chlooratomen aan de linkerkant (CL₂) en slechts één aan de rechterkant (KCL). Om dit in evenwicht te brengen, plaatsen we een coëfficiënt van 2 voor KCL.
* Nu zijn er twee kaliumatomen aan de rechterkant (2KCL), dus we plaatsen een coëfficiënt van 2 voor K aan de linkerkant.
Sleutelpunten:
* Chemische vergelijkingen moeten in evenwicht zijn om de wet van het behoud van massa te vertegenwoordigen.
* Balancering omvat het aanpassen van coëfficiënten (getallen voor de chemische formules) om hetzelfde aantal van elk type atoom aan beide zijden van de vergelijking te waarborgen.
 Wat is het aantal valentie-elektronen in natrium- of zuurstofionen?
Wat is het aantal valentie-elektronen in natrium- of zuurstofionen?  Wat stel je voor dat je 2 kleurloze oplossingen hebt gekregen beschrijven hoe kan erachter komen welke van hen de grotere concentratie die suiker vermindert?
Wat stel je voor dat je 2 kleurloze oplossingen hebt gekregen beschrijven hoe kan erachter komen welke van hen de grotere concentratie die suiker vermindert?  Hoe balanceert u natriumwaterstofcarbonaat gelijk aan natrium plus koolstofdioxidewater?
Hoe balanceert u natriumwaterstofcarbonaat gelijk aan natrium plus koolstofdioxidewater?  Kan ik die chemicaliën mengen? Daar is een app voor!
Kan ik die chemicaliën mengen? Daar is een app voor! Hoeveel formule-eenheden zitten er in 0,671 mol ijzer III-sulfaat?
Hoeveel formule-eenheden zitten er in 0,671 mol ijzer III-sulfaat?
Hoofdlijnen
- Onderzoek laat zien hoe de ineenstorting van eiwitprocessen veroudering en dood van de bestuurder veroorzaakt
- Hoe kan het gras op de greens op een golfbaan zo perfect zijn?
- Welke organel wordt biochemische machine genoemd en waarom?
- Geowetenschappers vergelijken micro-organismen in de poolgebieden
- Wat is een ander woord voor kenmerken in de wetenschap?
- Ademhaling bij zoogdieren
- Hoe 'Moeder van Duizenden' plantjes maakt
- Te ingewikkeld denken? Neuronale activiteit is veel voorspelbaarder dan aangenomen
- Cellen gestrest? Maak de mitochondriën langer
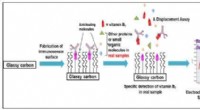
- Vitamine B7-bewakingsapparaat voor analyse van voedsel en klinische monsters
- Neutronen onthullen de wilde Weyl-wereld van halfmetalen

- Een beter begrip van de principes van siliciumetsen leidt tot verbeterde oppervlaktepatronen

- Molecuuleigenschappen veranderen door licht

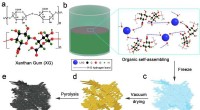
- Onderzoekers stellen nieuwe krachtige dual-ion-batterijen voor met een 3D-poreuze structuur
 Welke planeten hebben wolken?
Welke planeten hebben wolken?  Hoe polynomen op te lossen op een TI-84 Plus
Hoe polynomen op te lossen op een TI-84 Plus  Het type energie opgeslagen door fossiele brandstoffen zoals steenkool is?
Het type energie opgeslagen door fossiele brandstoffen zoals steenkool is?  Hoe het PH-niveau in water te verhogen
Hoe het PH-niveau in water te verhogen  Wat voor soort erosie buigt op de buitenkant een rivier?
Wat voor soort erosie buigt op de buitenkant een rivier?  Wat gebeurt er met gravitaionale kracht als de massa afneemt?
Wat gebeurt er met gravitaionale kracht als de massa afneemt?  Behandeling met plantenvirussen met nanodeeltjes is veelbelovend in de strijd tegen uitgezaaide kankers bij muizen
Behandeling met plantenvirussen met nanodeeltjes is veelbelovend in de strijd tegen uitgezaaide kankers bij muizen  Wat waren de 2 energiebronnen voorgesteld door de Oparin -theorie?
Wat waren de 2 energiebronnen voorgesteld door de Oparin -theorie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

