
Wetenschap
Hoeveel valentie-elektronen heeft CO3 2- heeft?
Hier leest u hoe u het aantal valentie -elektronen in het carbonaation (co₃²⁻) kunt bepalen:
1. Valentie -elektronen van individuele atomen:
* koolstof (c): Groep 14, 4 valentie -elektronen
* zuurstof (O): Groep 16, 6 valentie -elektronen
2. Totale valentie -elektronen (lading negeren):
* Koolstof:1 atoom * 4 elektronen =4 elektronen
* Zuurstof:3 atomen * 6 elektronen =18 elektronen
* Totaal:4 + 18 =22 elektronen
3. Rekening voor de kosten:
* De 2- lading geeft aan dat het ion twee extra elektronen heeft opgedaan.
* Voeg 2 toe aan het totaal:22 + 2 =24 elektronen
Daarom heeft het carbonaation (co₃²⁻) 24 valentie -elektronen.
Hoofdlijnen
- Wanneer wetenschappers items groeperen die op de een of andere manier hetzelfde zijn, zijn ze?
- Is de genetische informatie in dochtercellen uniek of indetisch?
- Wat is de slogeen voor schaal?
- Wat is de ultieme oorzaak van allelen?
- Hoe wordt DNA gebruikt in de microbiologie?
- wat heeft men nodig:zuurstof, cellulaire ademhaling of fermentatie?
- Het samenspel van genen geeft aanwijzingen over hoe nieuwe celtypen zouden kunnen evolueren
- Welke organel moet aanwezig zijn in grote aantallen in spiercellen?
- Hoe beïnvloeden het uitsterven van andere wezens mensen direct?
- Nieuwe connector voor duurzame constructies op aarde en in de ruimte

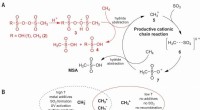
- Methaanoxidatie aan de positieve kant - Een selectieve industriële route naar methaansulfonzuur
- Katalytische reacties beheersen door nano-oppervlakken te veranderen

- Het nabootsen van het falen om de sterkte in composieten te vinden

- Watermoleculen splitsen voor een toekomst met hernieuwbare energie

 Welke twee planeten hebben gigantische stormen op zich?
Welke twee planeten hebben gigantische stormen op zich?  Wordt een droge cel in zaklamp een voorbeeld van mechanische energie gebruikt?
Wordt een droge cel in zaklamp een voorbeeld van mechanische energie gebruikt?  Hoe varieert de relatieve permeabiliteit van een ferromagnetisch materiaal met magnetomotorische kracht?
Hoe varieert de relatieve permeabiliteit van een ferromagnetisch materiaal met magnetomotorische kracht?  Wat zijn twee componenten van alle krachten?
Wat zijn twee componenten van alle krachten?  Wat bestaat alleen uit koolstofwaterstof en zuurstof?
Wat bestaat alleen uit koolstofwaterstof en zuurstof?  Natuurkundigen experimenteren met nanodraad in een veelbelovend veld dat elektronica kleiner zou kunnen maken, sneller en goedkoper
Natuurkundigen experimenteren met nanodraad in een veelbelovend veld dat elektronica kleiner zou kunnen maken, sneller en goedkoper Wat is het meervoud voor ruimtevaartuig?
Wat is het meervoud voor ruimtevaartuig?  Zware metalen openen pad naar nanomagneten op hoge temperatuur
Zware metalen openen pad naar nanomagneten op hoge temperatuur
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


