
Wetenschap
Hoeveel totale atomen zijn vereist om 60 g HNO3 voor te bereiden?
1. Bereken de molaire massa van HNO3:
* H:1.01 g/mol
* N:14.01 g/mol
* O:16.00 g/mol (x 3)
* Totale molaire massa:1.01 + 14.01 + (16.00 * 3) =63,02 g/mol
2. Bereken het aantal mol hno3:
* mol =massa / molaire massa
* mol =60 g / 63.02 g / mol
* mol ≈ 0,952 mol
3. Bereken het aantal moleculen van HNO3:
* moleculen =mol * Avogadro's nummer (6.022 x 10^23 moleculen/mol)
* Moleculen ≈ 0,952 mol * 6.022 x 10^23 moleculen/mol
* Moleculen ≈ 5.73 x 10^23 moleculen
4. Bereken het totale aantal atomen:
* Elk HNO3 -molecuul bevat 5 atomen (1 H + 1 N + 3 O)
* Totale atomen =moleculen * atomen per molecuul
* Totale atomen ≈ 5,73 x 10^23 moleculen * 5 atomen/molecuul
* Totale atomen ≈ 2,87 x 10^24 atomen
Daarom zijn ongeveer 2,87 x 10^24 atomen vereist om 60 g HNO3 te bereiden.
Hoofdlijnen
- Wat is het verschil tussen een bacteriële en virale infectie?
- Wat is het aantal chromosomen in een edelsteen?
- Naam van een beroemde dierenwetenschapper?
- Waarom is osmose belangrijk voor de celfunctie?
- Onderzoek laat zien hoe bloedcellen van vorm veranderen
- Hoe beïnvloeden Genotype en Fenotype hoe je eruit ziet?
- Appelbomen dragen meer fruit als ze omringd zijn door goede buren
- Wat is het doel van anxiolytica?
- Hoe laag strekt de biosfeer zich uit?
- Veel kleine verschillen dragen bij aan een grote variatie
- Complexe moleculen aan het werk zien
- Materialen voor waterstofservice ontwikkeld door nieuw multilab-consortium

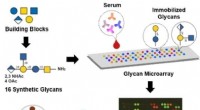
- Wetenschappers identificeren potentieel vaccindoelwit voor steeds meer bacteriestammen
- Milieuvriendelijke geluidsabsorbers maken van zeewier

 Wat is de volgorde van erosie door water?
Wat is de volgorde van erosie door water?  Hoe werken op zonne -energie op zonne -energie?
Hoe werken op zonne -energie op zonne -energie?  Hoe zien aurora’s eruit? | Hoe dingen werken
Hoe zien aurora’s eruit? | Hoe dingen werken  Bestaat de planeet Kepler echt?
Bestaat de planeet Kepler echt?  Wat hebben wetenschappers geleerd van experimenten die zijn ontworpen om de hypothese te testen dat leven uit niet-levende materialen is ontstaan?
Wat hebben wetenschappers geleerd van experimenten die zijn ontworpen om de hypothese te testen dat leven uit niet-levende materialen is ontstaan?  GECAM-team meldt eerste detectie van transiënten van gammastraling
GECAM-team meldt eerste detectie van transiënten van gammastraling Bestaat MySpace nog? Ja, en nu is Time Inc. eigenaar ervan (Update)
Bestaat MySpace nog? Ja, en nu is Time Inc. eigenaar ervan (Update)  Hoe luchtvaartpersoneel werkt
Hoe luchtvaartpersoneel werkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


