
Wetenschap
Waarom mengt een stof goed in water?
1. Polariteit:
* Water is een polair molecuul: Dit betekent dat het ene uiteinde van het molecuul een enigszins positieve lading heeft en het andere uiteinde een enigszins negatieve lading heeft. Dit creëert een "pull" of aantrekkingskracht tussen watermoleculen.
* "zoals oplost zoals": Stoffen die ook polair zijn, zoals suiker of zout, kunnen interageren met de positieve en negatieve uiteinden van watermoleculen. Hierdoor kan de stof uit elkaar breken en worden omringd door watermoleculen, effectief oplossen.
2. Waterstofbinding:
* Watermoleculen vormen waterstofbruggen: Dit is een sterk type aantrekkingskracht tussen het waterstofatoom van het ene watermolecuul en het zuurstofatoom van een ander.
* Polaire stoffen kunnen waterstofbruggen vormen met water: Dit verbetert verder het vermogen van deze stoffen om op te lossen.
3. Andere factoren:
* Temperatuur: Hogere temperaturen verhogen de kinetische energie van moleculen, waardoor ze sneller bewegen en het verbreken van bindingen in de stof vergemakkelijken en beter mengen mogelijk maken.
* Druk: Verhoogde druk kan meer moleculen in oplossing dwingen.
stoffen die niet goed samengaan met water:
* Niet-polaire stoffen: Deze stoffen hebben geen scheiding van ladingen en worden niet aangetrokken tot watermoleculen. Voorbeelden zijn olie, vet en was. Deze stoffen hebben de neiging om samen te klonteren of afzonderlijke lagen in water te vormen.
Key Takeaway: Het vermogen van een stof om op te lossen in water hangt voornamelijk af van zijn polariteit en zijn vermogen om waterstofbindingen te vormen met watermoleculen.
 Hoe ondersteunt mineraal bewijs Pangea?
Hoe ondersteunt mineraal bewijs Pangea?  Hoe kan de theoretische opbrengst van koolstofdisulfide worden berekend wanneer 120 g methaan wordt gereageerd met een gelijke massa -zwavel?
Hoe kan de theoretische opbrengst van koolstofdisulfide worden berekend wanneer 120 g methaan wordt gereageerd met een gelijke massa -zwavel?  Welk metaal reageert het heftigst met een zuur?
Welk metaal reageert het heftigst met een zuur?  Nieuwe methode gebruikt fluorescentie om ziekteverwekkende vormen van eiwitten te identificeren
Nieuwe methode gebruikt fluorescentie om ziekteverwekkende vormen van eiwitten te identificeren Wat bedoel je met de pH van een oplossing?
Wat bedoel je met de pH van een oplossing?
 Verbazingwekkende koeien zijn veelbelovend in baanbrekende duurzame voedselsystemen van de toekomst
Verbazingwekkende koeien zijn veelbelovend in baanbrekende duurzame voedselsystemen van de toekomst Tyfoon Trami gewond 50, klaart voltreffer op het vasteland van Japan
Tyfoon Trami gewond 50, klaart voltreffer op het vasteland van Japan Waarom zijn groene planten belangrijk voor het milieu?
Waarom zijn groene planten belangrijk voor het milieu?  Schildpadden die worden gevonden in Indiana
Schildpadden die worden gevonden in Indiana Hoe lang duurt het voordat een glazen fles wordt afgebroken in een stortplaats?
Hoe lang duurt het voordat een glazen fles wordt afgebroken in een stortplaats?
Hoofdlijnen
- Wat beschrijft correct een verschil tussen de mannelijke en vrouwelijke voortplantingssystemen?
- De twee of meer gerelateerde genen die een eigenschap regelen, staan bekend als?
- Wat gebeurt er als nieuwe gegevens de huidige wetenschappelijke verklaringen in Qeustion noemen?
- Wat is de beschermende barrière die alle cellen omsluit?
- Waar in het lichaam is vitamine D geproduceerd en uit welk molecuul wordt het gewijzigd?
- Gebruiken paddenstoelen echt taal om met elkaar te praten? Een schimmelexpert onderzoekt
- Om een visserij te beheren, moet je weten hoe de vissen sterven
- Waarom wordt DNA getranscribeerd?
- Hoe jasmonaatsignalering wordt verbeterd onder fosforarme omstandigheden in de plantenfysiologie
- Elektronische chip bootst de hersenen na om in een flits herinneringen te maken

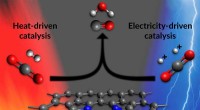
- Hoe een enkele katalysator op twee manieren koolstofdioxide in brandstof kan omzetten
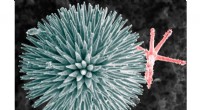
- Als je beter kijkt, zie je axiale filamenten in spicules van zeespons die uit eiwitten bestaan
- Grote moleculen uit voedingsvezels kunnen de darmomgeving veranderen door fysieke krachten
- Door ontwerp:van afval naar de volgende generatie koolstofvezel

 Thermische geleidbaarheid: definitie, eenheden, vergelijking & voorbeeld
Thermische geleidbaarheid: definitie, eenheden, vergelijking & voorbeeld  Hoeveel elektronen zijn er in een fosforatoom?
Hoeveel elektronen zijn er in een fosforatoom?  Uitgebreide modellering van waterbronnen toegankelijker maken
Uitgebreide modellering van waterbronnen toegankelijker maken Wat kan geweld veroorzaken in postkoloniaal Afrika?
Wat kan geweld veroorzaken in postkoloniaal Afrika?  Uit welk type kristal wordt gevormd in extrusieve stollingsgesteenten?
Uit welk type kristal wordt gevormd in extrusieve stollingsgesteenten?  Team ontwikkelt peptide dat resistente bacteriën weer gevoelig maakt voor antibiotica
Team ontwikkelt peptide dat resistente bacteriën weer gevoelig maakt voor antibiotica Wetenschappers onderzoeken eigenschappen van hybride systemen bestaande uit koolstofnanostructuren en een kleurstof
Wetenschappers onderzoeken eigenschappen van hybride systemen bestaande uit koolstofnanostructuren en een kleurstof Waterdruppels vormen grafeen nanostructuren
Waterdruppels vormen grafeen nanostructuren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

