
Wetenschap
Hoeveel atomen zijn er in 1.000 mol H2?
Hier leest u hoe u het aantal atomen in 1.000 mol H2 kunt achterhalen:
1. Avogadro's nummer:
* Het nummer van Avogadro vertelt ons het aantal deeltjes (atomen, moleculen, enz.) In één mol van een stof. Het is ongeveer 6.022 x 10^23 deeltjes/mol.
2. Moleculen versus atomen:
* H2 vertegenwoordigt een molecuul waterstofgas. Elk molecuul bevat twee waterstofatomen.
Berekening:
1. atomen per molecuul: Er zijn 2 waterstofatomen in één H2 -molecuul.
2. atomen per mol: Vermenigvuldig het nummer van Avogadro met het aantal atomen per molecuul:
(6.022 x 10^23 moleculen/mol) * (2 atomen/molecuul) =1.204 x 10^24 atomen
Antwoord: Er zijn 1.204 x 10^24 atomen In 1.000 mol H2.
 Wat is de tak van de wetenschap die van toepassing is op stoffen die koolstof bevatten die wordt genoemd?
Wat is de tak van de wetenschap die van toepassing is op stoffen die koolstof bevatten die wordt genoemd?  Waarom maakt natrium ionische binding met chloor?
Waarom maakt natrium ionische binding met chloor?  Hoeveel mol MGCL2 zijn er in 313 g de verbinding?
Hoeveel mol MGCL2 zijn er in 313 g de verbinding?  Wat is het atoomnummer van carbonaat?
Wat is het atoomnummer van carbonaat?  Wanneer aminozuren worden gedeamineerd, welke bron kunnen ze worden gebruikt?
Wanneer aminozuren worden gedeamineerd, welke bron kunnen ze worden gebruikt?
Hoofdlijnen
- Welke stoffen laten dingen in en uit de cel gaan?
- Wat heeft meer biomassa voor fotosynthetisch weefsel en minder ondersteunend weefsel?
- Het type celverbinding dat de inhoud voorkomt maag of urineblaas om in omliggende weefsels te lekken?
- Wat is intracellulaire bron van spijsverteringsenzymen?
- Forest Service weegt wijzigingen in bescherming voor saliehoen af
- Hebben dierencellen en planten een celmembraan?
- In een plant zouden de reproductieve organen worden gevonden?
- Wat scheiden alfacellen af?
- Wat heeft uw lichaam nodig om te groeien en zichzelf te herstellen?
- Video:Hoe de houdbaarheidsdatum van medicijnen werkt

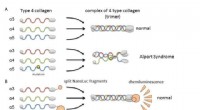
- Een zeer gevoelig en multi-analytisch systeem voor erfelijke nierziekte
- Gasopslagmethode kan de volgende generatie schone energievoertuigen helpen

- Onderzoekers verbeteren de mechanische eigenschappen van aluminium/stalen verbindingen
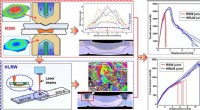
- Een snel en goedkoop apparaat om virussen op te vangen en te identificeren
 Hoeveel pond in 18.500 kg?
Hoeveel pond in 18.500 kg?  Wordt de winterzonnewende naar de zon gekanteld?
Wordt de winterzonnewende naar de zon gekanteld?  Luistert Facebook naar mij? Waarom die advertenties verschijnen nadat je over dingen hebt gesproken
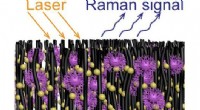
Luistert Facebook naar mij? Waarom die advertenties verschijnen nadat je over dingen hebt gesproken Optische geheimen van disulfide nanobuisjes worden onthuld
Optische geheimen van disulfide nanobuisjes worden onthuld Verandert een verandering in de richting van de snelheid?
Verandert een verandering in de richting van de snelheid?  Wat classificeer je in de wetenschap?
Wat classificeer je in de wetenschap?  Hoe mineraalwater verschilt van gedestilleerd water?
Hoe mineraalwater verschilt van gedestilleerd water?  Hoe kunnen de maankraters en Rilles zich hebben gevormd?
Hoe kunnen de maankraters en Rilles zich hebben gevormd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

