
Wetenschap
Wat is de chemische reactie voor oplossingen voor zilvernitraat en kaliumchromaat?
2AGNO₃ (aq) + k₂cro₄ (aq) → ag₂cro₄ (s) + 2Kno₃ (aq)
Hier is een uitsplitsing van de reactie:
* reactanten:
* zilvernitraat (agno₃): Een kleurloze, oplosbare ionische verbinding.
* kaliumchromaat (k₂cro₄): Een gele, oplosbare ionische verbinding.
* Producten:
* zilveren chromaat (ag₂cro₄): Een roodbruine, onoplosbare vast neerslag.
* kaliumnitraat (kno₃): Een kleurloze, oplosbare ionische verbinding.
Verklaring:
* De zilverionen (Ag⁺) van zilvernitraat reageren met de chromaationen (Cro₄²⁻) van kaliumchromaat om zilverchromaat te vormen (Ag₂cro₄).
* Omdat zilverchromaat onoplosbaar is in water, gaat het uit de oplossing, waardoor de roodbruine vaste stof ontstaat.
* De kaliumionen (k⁺) en nitraationen (no₃⁻) blijven in oplossing als kaliumnitraat, dat oplosbaar is.
Key Observations:
* Vorming van een roodbruin neerslag.
* De oplossing verandert van kleur van aanvankelijk kleurloos in een geelachtige tint vanwege de aanwezigheid van chromaationen.
Deze reactie is een klassiek voorbeeld van een neerslagreactie en wordt vaak gebruikt in kwalitatieve analyse om de aanwezigheid van zilverionen of chromaationen in een oplossing te identificeren.
 Geschillen over klimaatverandering groeien snel, zegt wereldwijde studie
Geschillen over klimaatverandering groeien snel, zegt wereldwijde studie Treffen tornado's onevenredig veel caravanparken?
Treffen tornado's onevenredig veel caravanparken?  Fosfor is van vitaal belang voor het leven op aarde - en was bijna op
Fosfor is van vitaal belang voor het leven op aarde - en was bijna op Indringende vraag:Wat komt eerst:de woorden of de muziek?
Indringende vraag:Wat komt eerst:de woorden of de muziek?  Wat is de beste beschrijving van alle onderwerpen die zijn bestudeerd in de aardewetenschap?
Wat is de beste beschrijving van alle onderwerpen die zijn bestudeerd in de aardewetenschap?
Hoofdlijnen
- Hoe biologen veldwerk veiliger en rechtvaardiger maken
- Welk type micro -organisme maakte de chemische stof die bacteriën op plaat doodde?
- Hoe je winnaar kunt worden in het evolutiespel
- Wat zijn constante factoren in de wetenschap?
- Light frisdrank en friet, alstublieft:hoe consumenten hun voedselkeuzes in evenwicht brengen
- Wat zijn de drie soorten modellen die door wetenschappers worden gebruikt?
- Wat is het doel van een spore?
- Wat hebben rommelige gazons te maken met bijenvoer? Een deskundige legt het uit
- Onderzoekers onthullen hoe planten zichzelf beschermen tegen virale infecties door deacetylering te reguleren
- Nieuw materiaal breekt wereldrecord voor het omzetten van warmte in elektriciteit

- 3D-afbeeldingen van stoffen sandwich kunnen helpen bij het meten van textielwrijving

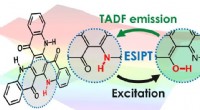
- Gebruik maken van hoppende waterstofatomen voor zeer efficiënte OLED's
- Engineering van een nieuwe draai voor ziektediagnostiek

- Video:Waarom plastic flessen worden gerecycled tot kleding

 NASA legt uit waarom 30 juni een extra seconde krijgt
NASA legt uit waarom 30 juni een extra seconde krijgt  Floridas oesters in Apalachicola, Cedar Key wordt geconfronteerd met klimaatbedreigingen voor overleving
Floridas oesters in Apalachicola, Cedar Key wordt geconfronteerd met klimaatbedreigingen voor overleving Trump kan stappen ondernemen om de VS uit de klimaatovereenkomst van Parijs te halen
Trump kan stappen ondernemen om de VS uit de klimaatovereenkomst van Parijs te halen Californië verlaagt kortingen op elektrische auto's laat luxe modellen vallen
Californië verlaagt kortingen op elektrische auto's laat luxe modellen vallen Wat is Rock en hoe beweegt het?
Wat is Rock en hoe beweegt het?  NASA's Juno onthult donkere oorsprong van een van Jupiters grote lichtshows
NASA's Juno onthult donkere oorsprong van een van Jupiters grote lichtshows Valt energie onder de fysieke wetenschap?
Valt energie onder de fysieke wetenschap?  Huisvestingskosten drukken de tevredenheid van bewoners met het leven in Los Angeles
Huisvestingskosten drukken de tevredenheid van bewoners met het leven in Los Angeles
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

