
Wetenschap
Waarom hebben zwavel en zuurstof verschillende chemische eigenschappen?
1. Elektronische configuratie:
* zuurstof: Zuurstof heeft de elektronische configuratie 1S² 2S² 2P⁴. Het heeft zes valentie -elektronen (elektronen in de buitenste schaal), waardoor het zeer elektronegatief is en graag twee elektronen kan krijgen om een stabiele octetconfiguratie te bereiken.
* zwavel: Zwavel heeft de elektronische configuratie 1S² 2S² 2P⁶ 3S² 3P⁴. Het heeft ook zes valentie -elektronen, maar ze bevinden zich in een hoger energieniveau (3p) in vergelijking met zuurstof. Dit maakt zwavel minder elektronegatief dan zuurstof.
2. Atomic Grootte:
* zuurstof: Zuurstof is een kleiner atoom dan zwavel, met een kleinere atoomradius. Dit zorgt ervoor dat de valentie -elektronen van Oxygen strakker worden vastgehouden door de kern, wat leidt tot hogere elektronegativiteit.
* zwavel: Zwavel is een groter atoom met een grotere atoomradius. De valentie -elektronen zijn verder van de kern en ervaren dus een zwakkere aantrekkingskracht, wat resulteert in een lagere elektronegativiteit.
3. Ionisatie -energie:
* zuurstof: Zuurstof heeft een hogere ionisatie -energie dan zwavel, wat betekent dat het meer energie vereist om een elektron uit de buitenste schaal te verwijderen. Dit komt door de kleinere grootte en sterkere aantrekkingskracht tussen de kern- en valentie -elektronen.
* zwavel: Zwavel heeft een lagere ionisatie -energie vanwege zijn grotere omvang en zwakkere aantrekkingskracht tussen de kern- en valentie -elektronen.
4. Oxidatie stelt:
* zuurstof: Zuurstof vertoont typisch oxidatietoestanden van -2, hoewel het ook andere oxidatietoestanden kan hebben, zoals -1 in peroxiden.
* zwavel: Zwavel vertoont een breder bereik van oxidatietoestanden, van -2 tot +6. Dit komt omdat de valentie -elektronen verder van de kern zijn en kunnen deelnemen aan een grotere verscheidenheid aan bindingsinteracties.
5. Reactiviteit:
* zuurstof: Zuurstof is een zeer reactief element vanwege de sterke elektronegativiteit en de neiging om twee elektronen te krijgen om stabiele oxiden te vormen.
* zwavel: Zwavel is minder reactief dan zuurstof, maar vormt nog steeds verbindingen met verschillende elementen, zoals sulfiden en sulfaten.
6. Bindingsvoorkeuren:
* zuurstof: Zuurstof vormt gemakkelijk dubbele bindingen (O =O in O₂) en neemt deel aan waterstofbinding.
* zwavel: Zwavel vormt gemakkelijker enkele bindingen (S-S in S₈) en kan meerdere bindingen vormen, maar met minder frequentie dan zuurstof.
Deze verschillen in elektronische configuratie, atoomgrootte, ionisatie -energie, oxidatietoestanden, reactiviteit en bindingsvoorkeuren resulteren in de verschillende chemische eigenschappen die worden waargenomen tussen zuurstof en zwavel.
 Snelle meting van aërosolvluchtigheid met behulp van een op deep learning gebaseerde draagbare microscoop
Snelle meting van aërosolvluchtigheid met behulp van een op deep learning gebaseerde draagbare microscoop Waar is een Ant-Atueel van gemaakt?
Waar is een Ant-Atueel van gemaakt?  Hoe heet de compound Tiso4?
Hoe heet de compound Tiso4?  Hoe Polycomb repressieve deubiquitinase specifiek de ubiquitinatie van H2AK119 op het nucleosoom verwijdert
Hoe Polycomb repressieve deubiquitinase specifiek de ubiquitinatie van H2AK119 op het nucleosoom verwijdert  ARS Cotton Advance helpt bij het lanceren van wondverband
ARS Cotton Advance helpt bij het lanceren van wondverband
 Wat u moet weten over de watersystemen in Dallas en nieuwe federale limieten voor forever-chemicaliën
Wat u moet weten over de watersystemen in Dallas en nieuwe federale limieten voor forever-chemicaliën  Planten en dieren die leven in de buurt van de Koalas Habitat
Planten en dieren die leven in de buurt van de Koalas Habitat Nieuwe tool ondersteunt toekomst van biologische landbouw
Nieuwe tool ondersteunt toekomst van biologische landbouw Wat is de naam van de wetenschap die zich bezighoudt met dynamiek en fysieke geschiedenis aarde?
Wat is de naam van de wetenschap die zich bezighoudt met dynamiek en fysieke geschiedenis aarde?  Echte weerterm bom ontploft op sociale media
Echte weerterm bom ontploft op sociale media
Hoofdlijnen
- Wat zijn alle bionomen?
- Wat is de naam van de ziekte waarin het lichaam van defecte cellen blijft verdelen op een ongecontroleerde manier?
- Wat is de rol van waterstof in levende organismen?
- Wat is het enige menselijke orgaan dat zichzelf regenereert?
- Onderscheid u van de kudde:hoe koeien communiceren gedurende hun leven
- Hoe bacteriën hun celcyclus controleren
- Welke cel kan een stof transporteren als deze te groot is om membraan te kruisen?
- Kamgelei mogelijk eerste afstamming van evolutionaire boom
- Waarom moeten cellen delen?
- Het licht zien:onderzoekers bieden oplossing voor efficiëntieprobleem van kunstmatige fotosynthese
- Dankzij subtiele ioninteracties op moleculair niveau kunnen wetenschappers het smeltpunt van ionische verbindingen afstemmen
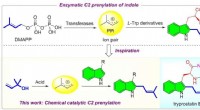
- Bio-geïnspireerde door zuur gekatalyseerde C2-prenylatie van indoolderivaten
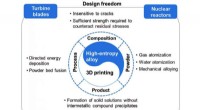
- Onderzoekers beoordelen de vooruitgang in 3D-printen van legeringen met hoge entropie
- Nieuwe techniek maakt de weg vrij voor perfecte perovskieten

 Hoe maak je zink en aluminium op Alchemy Classic?
Hoe maak je zink en aluminium op Alchemy Classic?  In welk sterrenbeeld zit er een sterrenstelsel?
In welk sterrenbeeld zit er een sterrenstelsel?  Wat is de ionische formule als waterig hypochloreus zuur en waterige calciumhydroxide reageren?
Wat is de ionische formule als waterig hypochloreus zuur en waterige calciumhydroxide reageren?  Satellieten laten winst zien in het water in Californië
Satellieten laten winst zien in het water in Californië  Is het universum werkelijk een ‘donker bos’ vol vijandige buitenaardse wezens die zich schuilhouden?
Is het universum werkelijk een ‘donker bos’ vol vijandige buitenaardse wezens die zich schuilhouden?  de geometrie van accretieschijven voor nucleaire zwarte gaten
de geometrie van accretieschijven voor nucleaire zwarte gaten Milieuvriendelijke zonnecellen verbeteren de efficiëntie van energieopwekking door defecten op te lossen
Milieuvriendelijke zonnecellen verbeteren de efficiëntie van energieopwekking door defecten op te lossen Oude inheemse Nieuw-Mexicaanse gemeenschap wist duurzaam samen te leven met bosbranden
Oude inheemse Nieuw-Mexicaanse gemeenschap wist duurzaam samen te leven met bosbranden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

