
Wetenschap
De geometrie van een waterstofbromidemolecuul is?
De geometrie van een waterstofbromide (HBR) molecuul is lineair .
Dit is waarom:
* binding: HBR vormt een enkele covalente binding tussen het waterstofatoom en het broomatoom.
* elektronegativiteit: Bromine is elektronegatiefer dan waterstof, wat betekent dat het de gedeelde elektronen in de binding sterker aantrekt.
* eenzame paren: Bromine heeft drie eenzame paar elektronen.
Vanwege de enkele binding en de enige paren op broom, zijn er geen krachten die de atomen uit een rechte lijn duwen of trekken. Dit resulteert in een lineaire geometrie.
 Welke vloeistof wordt een gas bij 100 graden Celsius?
Welke vloeistof wordt een gas bij 100 graden Celsius?  Wat is de reactiviteit van cesium?
Wat is de reactiviteit van cesium?  Wat zijn vijf veel voorkomende stoffen die worden beschouwd als organische chemicaliën?
Wat zijn vijf veel voorkomende stoffen die worden beschouwd als organische chemicaliën?  Vormt koper een covalente verbinding?
Vormt koper een covalente verbinding?  Waarom denk je dat waterstof in het verleden werd gebruikt om Zeppelins blimps luchtlucht te laten zweven?
Waarom denk je dat waterstof in het verleden werd gebruikt om Zeppelins blimps luchtlucht te laten zweven?
 Feiten over meelwormen voor kinderen
Feiten over meelwormen voor kinderen  Afbeelding:Het vuur van Thomas blijft groeien, maar het weer kan de inspanningen helpen
Afbeelding:Het vuur van Thomas blijft groeien, maar het weer kan de inspanningen helpen Soorten Schorpioenen Native to Colorado
Soorten Schorpioenen Native to Colorado  Leeftijd is meer dan een getal:bij kerkuilen laat het zien hoe vatbaar iemand is voor klimaatverandering
Leeftijd is meer dan een getal:bij kerkuilen laat het zien hoe vatbaar iemand is voor klimaatverandering  Brandweerlieden bestrijden tweede natuurbrand in Noord-Engeland
Brandweerlieden bestrijden tweede natuurbrand in Noord-Engeland
Hoofdlijnen
- Wat is pleoitophs?
- Eerste structurele inzichten in hoe immuunreceptoren van planten op elkaar inwerken
- Pissebedden hebben het nieuwe record voor de kleinste verspreiders van ingenomen zaden
- Waarom moet een gamete allel uit elk gen dragen?
- Welke cel heeft een of meer grote vacuolen?
- Het andere pad van de keel leidt tot longen dat het wordt genoemd?
- Wat is de rol van evenaar bij mitose?
- In welke biomen leven konijnen?
- Vloeistofdruppeltjes bepalen hoe cellen reageren op verandering, blijkt uit onderzoek
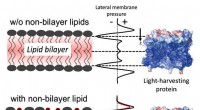
- Team ontdekt een mechanisme dat planten gebruiken om fotosynthese in te schakelen
- Studie vergroot wat we weten over natuurlijke, goedkope manieren om verontreinigende stoffen uit water te verwijderen

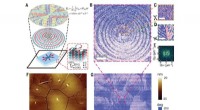
- Concentrische cirkelvormige polarisatiebanden gevonden in een ferro-elektrisch polymeer
- Zeer efficiënte methode om polyisopreenrubber met ultrahoog molecuulgewicht te synthetiseren

- Onderzoekers ontdekken nieuwe elektrokatalysator om koolstofdioxide om te zetten in vloeibare brandstof

 Hoe schoon kan een wijnstok een cent opbrengen?
Hoe schoon kan een wijnstok een cent opbrengen?  Onderzoeker:Waarom vakanties met familie vol conflicten kunnen zijn
Onderzoeker:Waarom vakanties met familie vol conflicten kunnen zijn Wat hebben osmose en diffusie gemeen?
Wat hebben osmose en diffusie gemeen?  Welvaartskloof tussen sociale huurders en het landelijk gemiddelde wordt kleiner, nieuw onderzoek toont aan
Welvaartskloof tussen sociale huurders en het landelijk gemiddelde wordt kleiner, nieuw onderzoek toont aan Wat zijn de drie manieren waarop warmte wordt overgedragen?
Wat zijn de drie manieren waarop warmte wordt overgedragen?  Ontgrendelen van effecten op pakketgeheugens op wetenschappelijke kernels met hoge prestaties
Ontgrendelen van effecten op pakketgeheugens op wetenschappelijke kernels met hoge prestaties Wat is Sabacious Bland?
Wat is Sabacious Bland?  Een wet alleen voor het presidentschap van Trump? De Californische maatregel heeft tot doel het milieu van de staat te beschermen
Een wet alleen voor het presidentschap van Trump? De Californische maatregel heeft tot doel het milieu van de staat te beschermen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

